Участие макрофагов в воспалении
Клетки участвующие в хроническом воспалении — макрофаги и другие клетки
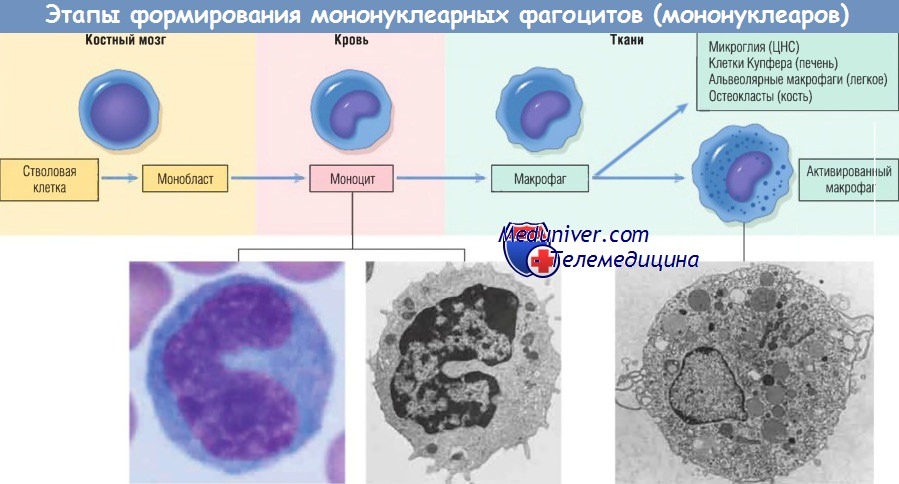
Макрофаг — главная клетка, участвующая в процессе хронического воспаления. Макрофаги являются частью системы мононуклеарных фагоцитов (иногда называемой ретикулоэндотелиальной системой), состоящей из клеток, близкородственных клеткам костного мозга, включая моноциты и тканевые макрофаги.
Тканевые макрофаги диффузно разбросаны по соединительной ткани или расположены в таких органах, как печень (клетки Купфера), селезенка и лимфатические узлы (гистиоциты синусов), легкие (альвеолярные макрофаги), а также в ЦНС (микроглия). Мононуклеарные фагоциты происходят из клеток-предшественников костного мозга, которые дифференцируются в моноциты. Из крови моноциты мигрируют в разные ткани и дифференцируются в макрофаги.
Период полужизни моноцитов длится около 1 дня, когда как период жизни тканевых макрофагов составляет несколько месяцев или лет. Превращение стволовой клетки костного мозга в тканевый макрофаг регулируется различными факторами роста и дифференцировки, цитокинами, молекулами адгезии и клеточными взаимодействиями.
Моноциты начинают мигрировать во внесосудистые ткани на ранних стадиях развития острого воспаления и в течение 48 час могут стать доминирующим типом клеток инфильтрата. Экстравазация моноцитов управляется теми же стимулами, которые участвуют в миграции нейтрофилов и представлены молекулами адгезии и химическими медиаторами с хемотаксическими и активирующими свойствами.
При попадании моноцита во внесосудистую ткань он подвергается трансформации в большую фагоцитарную клетку — макрофаг. Макрофаги активируются различными стимулами, включая микробные продукты, активирующие TLR и другие клеточные рецепторы, цитокины (например, IFN-y), секретированные сенсибилизированными Т-лимфоцитами и естественными клетками-киллерами, и другие химические медиаторы.
В результате активации макрофагов происходят элиминация таких повреждающих агентов, как микробы, и инициация процессов репарации, а также повреждение ткани (при хроническом воспалении).
Активация макрофагов приводит также к повышению уровней лизосомных ферментов и активных форм кислорода и азота, продукции цитокинов, факторов роста и других медиаторов воспаления. Некоторые из этих продуктов токсичны для микробов и организма (например, активные формы кислорода и азота) или ВКМ (протеазы); другие вызывают миграцию клеток (например, цитокины, хемотаксический стимул); третьи влияют на пролиферацию фибробластов, отложение коллагена и ангиогенез (например, факторы роста).
Разные популяции макрофагов выполняют различные функции: некоторые необходимы при киллинге микробов и воспалении, другие очень важны при репарации.
Впечатляющий арсенал медиаторов делает макрофаги мощным союзником организма в защите от непрошеных гостей, но в то же время при неправильной активации макрофаги могут вызывать значительное разрушение ткани, которое является одним из признаков хронического воспаления. Процесс разрушения ткани сам по себе может активировать каскад воспалительной реакции, поэтому одновременно могут присутствовать признаки и острого, и хронического воспаления.
При недолгом процессе воспаления, если стимул удален, макрофаги в итоге либо умирают, либо уходят в лимфатические сосуды и лимфоузлы. При хроническом воспалении происходит накопление макрофагов в результате их мобилизации из кровотока и местной пролиферации в очагах воспаления.
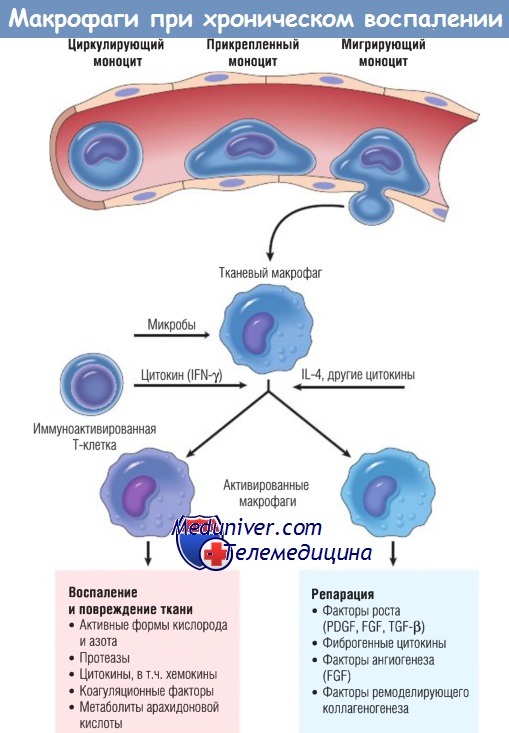
Роль активированных макрофагов при хроническом воспалении.
Макрофаги активируются неиммунными стимулами, например эндотоксином, или цитокинами из иммуноактивированных Т-клеток (особенно IFN-y).
Перечислена продукция активированных макрофагов.
FGF — фактор роста фибробластов; IFN — интерферон; IL — интерлейкин;
PDGF — тромбоцитарный фактор роста; TGF — трансформирующий фактор роста.
В развитии хронического воспаления участвуют и другие типы клеток: лимфоциты, клетки плазмы крови, эозинофилы и тучные клетки:
— лимфоциты мобилизуются в ходе как антителоопосредованных, так и клеточно-опосредованных иммунных реакций. Антиген-стимулированные лимфоциты (эффекторные клетки и клетки памяти) различных типов (Т- и В-клетки) используют разные пары адгезивных молекул (селектинов, интегринов и их лигандов) и хемокины для миграции в очаг воспаления. Цитокины активированных макрофагов, в основном TNF, IL-1 и хемокины, усиливают мобилизацию лейкоцитов, запуская стадию персистенции воспалительной реакции.
Лимфоциты и макрофаги взаимодействуют по реверсивному типу, что играет важную роль в развитии хронического воспаления. Макрофаги презентируют антигены Т-клеткам и продуцируют мембранные молекулы (костимуляторы) и цитокины (например, IL-12), которые стимулируют ответ Т-клеток. Активированные Т-клетки продуцируют цитокины, некоторые из которых мобилизуют моноциты из кровотока, и IFN-y — мощный активатор макрофагов. В результате этих взаимодействий Т-клеток и макрофагов в воспалительную реакцию вовлекается иммунная система, что делает реакцию хронической и тяжелой. Термин «иммунное воспаление» отражает наличие выраженного иммунного компонента в воспалительном процессе, например ответа Т- и В-клеток;
— клетки плазмы крови образуются из активированных В-клеток и продуцируют антитела, направленные либо против персистирующих чужеродных или собственных антигенов в очаге воспаления, либо против компонентов поврежденной ткани. При некоторых сильных воспалительных реакциях скопление лимфоцитов, антигенпрезентирующих клеток и клеток плазмы крови может напоминать морфологическое строение лимфоидного органа, особенно лимфоузла, содержащего хорошо сформированные герминативные центры.
Подобные очаги скопления лимфоцитов называют третичными лимфоидными органами. Такой тип лимфоидного органогенеза часто встречается в синовиальных оболочках у пациентов, длительно страдающих ревматоидным артритом;
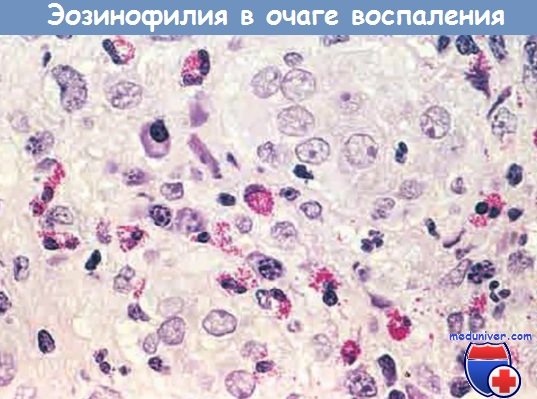
— эозинофилами изобилуют иммунные реакции, опосредованные IgE и паразитарными инфекциями. Особо важный хемокин для мобилизации эозинофилов — эотаксин. Эозинофилы содержат гранулы, имеющие главный основной белок (высокоактивный катионный белок), который токсичен для паразитов, но может вызвать лизис эпителиальных клеток млекопитающих. Таким образом, эозинофилы контролируют паразитарные инфекции, но также участвуют в повреждении ткани при иммунных реакциях, например аллергии;
— тучные клетки широко распространены в соединительных тканях по всему телу и могут участвовать как в острых, так и в хронических воспалительных реакциях. Тучные клетки экспрессируют на своей поверхности рецептор FceRI, связывающийся с Fc-фракцией антитела IgE. При реакции гиперчувствительности немедленного типа антитела IgE связываются с клеточными Fc-peцепторами, специфично распознающими антиген, клетка дегранулируется и высвобождает медиаторы — гистамин и простагландины. Этот тип ответа наблюдается при пищевой аллергии, укусах насекомых, лекарственной аллергии, иногда с ужасающими исходами (например, анафилактическим шоком).
Тучные клетки тоже присутствуют при реакциях хронического воспаления и секретируют множество цитокинов, т.е. они способны как усиливать, так и ограничивать воспалительную реакцию в разных ситуациях.
Как правило, присутствие нейтрофилов характерно для острого воспаления, но и при многих формах хронического воспаления, длящегося месяцами, выявляется большое количество нейтрофилов, индуцированных либо персистирующими микробами, либо медиаторами, продуцированными активированными макрофагами и Т-лимфоцитами. При хронических бактериальных инфекциях костей (остеомиелите) нейтрофильный экссудат может сохраняться многие месяцы. Нейтрофилы также важны при хроническом воспалении в легких, индуцированном курением или другим стимулом.
Помимо мононуклеарного характера клеточного инфильтрата при хроническом воспалении часто происходит пролиферация кровеносных и лимфатических сосудов. Этот процесс стимулируют факторы роста, продуцируемые макрофагами и эндотелиальными клетками.

Очаг воспаления с большим количеством эозинофилов (эозинофилия)
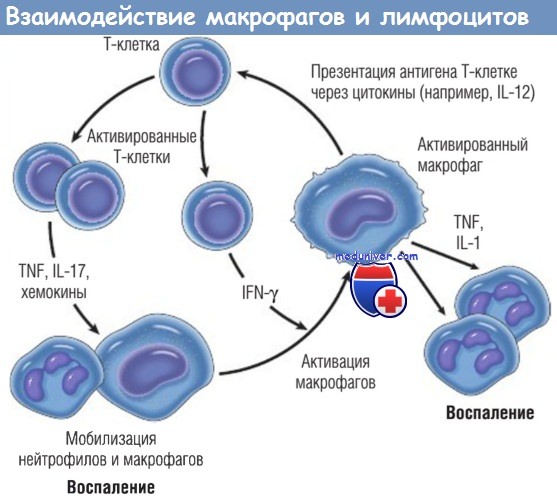
Взаимодействия макрофагов и лимфоцитов при хроническом воспалении.
Активированные Т-клетки продуцируют цитокины, которые мобилизуют макрофаги (TNF, IL-17, хемокины), и IFN-y, который является мощным активатором макрофагов.
Разные типы Т-клеток (Тh1 и Тh17) могут продуцировать различные типы цитокинов.
В свою очередь, активированные макрофаги стимулируют Т-клетки, презентируя им антигены через цитокины (например, IL-12).
IFN — интерферон; IL — интерлейкин; TNF — фактор некроза опухоли.
— Рекомендуем ознакомиться со следующей статьей «Причины и механизмы гранулематозного воспаления. Что такое гранулема?»
Оглавление темы «Патофизиология»:
- Клетки участвующие в хроническом воспалении — макрофаги и другие клетки
- Причины и механизмы гранулематозного воспаления. Что такое гранулема?
- Влияние воспаления на организм в целом (системные симптомы воспаления)
- Варианты воспалительной реакции и ее последствия
- Пути заживления и обновления тканей — репарация, регенерация
- Регуляция деления и пролиферации клеток в тканях
- Виды стволовых клеток и их характеристика
- Эмбриональные стволовые клетки и их характеристика
- Индуцированные плюрипотентные стволовые клетки (ИПСК) и их характеристика
- Где присутствуют стволовые клетки у взрослых?
Источник
Основная роль в развитии и поддержании хронического воспаления принадлежит системе фагоцитирующих макрофагов (это понятие заменило широко применявшийся ранее, но по существу недостаточно обоснованный термин «ретикулоэндотелиальная система»). Основная клетка этой системы—макрофаг, развившийся из моноцита крови. Моноциты, происходящие из стволовой клетки костного мозга, поступают вначале в периферическую кровь, а из нее в ткани, где под влиянием различных местных стимулов превращаются в макрофаги.
Последние имеют чрезвычайно большое значение в осуществлении адаптивных реакций организма — иммунных, воспалительных и репаративных. Участию в подобных реакциях способствуют такие биологические свойства макрофагов, как способность мигрировать в очаги воспаления, возможность быстрого и стойкого увеличения продукции клеток костным мозгом, активный фагоцитоз чужеродного материала с быстрым расщеплением последнего, активация под действием чужеродных стимулов, секреция ряда биологически активных веществ, способность «обрабатывать» проникший в организм антиген с последующей индукцией иммунного процесса.
Принципиально важно также, что макрофаги являются долгоживущими клетками, способными длительно функционировать в воспаленных тканях. Существенно, что они способны пролиферировать в очагах воспаления; при этом возможна трансформация макрофагов в эпителиоидные и гигантские многоядерные клетки.
Не обладая иммунологической специфичностью (как Т- и В-лимфоциты), макрофаг действует в качестве неспецифической вспомогательной клетки, обладающей уникальной способностью не только захватывать антиген, но и обрабатывать его так, что последующее распознавание этого антигена лимфоцитами значительно облегчается. Этот этап особенно необходим для активации Т-лимфоцитов (для развития иммунных реакций замедленного типа и для продукции антител к тимусзависимым антигенам).
Кроме участия в иммунных реакциях за счет предварительной обработки антигена и его последующего «представления» лимфоцитам, макрофаги осуществляют защитные функции и более непосредственно, уничтожая некоторые микроорганизмы, грибы и клетки опухолей.
Таким образом, при ревматических заболеваниях в клеточных реакциях иммунного воспаления участвуют не только специфически иммунизированные лимфоциты, но и не имеющие иммунологической специфичности моноциты и макрофаги.
Эти клетки привлекаются моноцитарными хемотаксическими веществами, вырабатываемыми в очагах воспаления. К ним относятся С5а, частично денатурированные белки, калликреин, активатор плазминогена, основные белки из лизосом нейтрофилов Т-лимфоциты вырабатывают подобный фактор при контакте ее специфическим антигеном, В-лимфоциты — с иммунными комплексами.
Кроме того, лимфоциты продуцируют также факторы угнетающие миграцию макрофагов (т. е. фиксирующие их в очаге воспаления) и активирующие их функцию. В воспалительных очагах в отличие от нормальных условий наблюдаются митозы макрофагов и таким образом количество этих клеток нарастает также за счет местной пролиферации.
Значение макрофагов в поддержании воспалительного процесса определяется рассматриваемыми ниже противовоспалительными агентами, освобождаемыми из этих клеток.
1. Простагландины.
2. Лизосомные ферменты (в частности, при фагоцитозе комплексов антиген — антитело, причем клетка при их выделении не разрушается).
3. Нейтральные протеазы (активатор плазминогена, коллагеназа, эластаза). В норме их количество ничтожно, но при чужеродной стимуляции (при фагоцитозе) продукция данных ферментов индуцируется и они выделяются в значительных количествах. Продукция нейтральных протеаз угнетается ингибиторами белкового синтеза, в том числе глюкокортикостероидами. Выработка активатора плазминогена и коллагеназы стимулируется также факторами, секретируемыми активированными лимфоцитами.
4. Фосфолипаза Аз, освобождающая из более сложных комплексов арахидоновую кислоту — основной предшественник простагландинов. Активность этого фермента тормозится глюкокортикостероидами.
5. Фактор, стимулирующий освобождение из костей как минеральных солей, так и органической основы костного матрикса. Этот фактор реализует свое влияние на костную ткань за счет прямого воздействия, не требуя присутствия остеокластов.
6. Ряд компонентов комплемента, которые активно синтезируются и выделяются макрофагами: С3, С4, С2 и, по-видимому, также С1 и фактор В, необходимый для альтернативного пути активирования комплемента. Синтез этих компонентов повышается при активировании макрофагов и тормозится ингибиторами белкового синтеза.
7. Интерлейкин-1, который является типичным представителем цитокинов — биологически активных веществ полипептидной природы, вырабатываемых клетками (прежде всего клетками иммунной системы). В зависимости от источников продукции этих веществ (лимфоциты или моноциты) нередко применяются термины «лимфокины» и «монокины». Название «интерлейкин» с соответствующим номером используется для обозначения конкретных цитокинов — особенно тех, которые опосредуют клеточное взаимодействие. Пока не вполне ясно, представляет ли интерлейкин-1, являющийся наиболее важным монокином, одно вещество или семейство полипептидов, обладающих очень близкими свойствами.
К этим свойствам относятся следующие:
- стимуляция В-клеток, ускоряющих их трансформацию в плазматические клетки;
- стимуляция активности фибробластов и синовиоцитов с повышенной выработкой ими простагландинов и коллагеназы;
- пирогенное влияние, реализующееся в развитии лихорадки;
- активирование синтеза в печени острофазовых белков, в частности сывороточного предшественника амилоида (этот эффект, возможно, является опосредованным — благодаря стимуляции выработки интерлейкина-6).
Среди системных эффектов интерлейкина-1, помимо лихорадки, могут быть отмечены также нейтрофилез и протеолиз скелетных мышц.
8. Интерлейкин-6, который также активирует В-клетки, стимулирует гепатоциты к выработке острофазовых белков и обладает свойствами b-интерферона.
9. Колониестимулирующие факторы, способствующие образованию в костном мозге гранулоцитов и моноцитов.
10. Фактор некроза опухолей (ФНО), который не только действительно способен вызывать некроз опухолей, но и играет заметную роль в развитии воспаления. Этот полипептид, состоящий из 157 аминокислот, в раннюю фазу воспалительной реакции способствует прилипанию нейтрофилов к эндотелию и способствует тем самым их проникновению в очаг воспаления. Он служит также мощным сигналом к выработке токсичных кислородных радикалов и является стимулятором В-клеток, фибробластов и эндотелия (2 последних типа клеток при этом вырабатывают колониестимулирующие факторы).
Клинически важно, что ФНО, так же как интерлейкин-1 и интерферон, подавляют активность липопротеинлипазы, которая обеспечивает отложение жира в организме. Именно поэтому при воспалительных заболеваниях часто отмечается выраженное похудание, не соответствующее калорийному питанию и сохранившемуся аппетиту. Отсюда второе название ФНО — кахектин.
Активация макрофагов, проявляющаяся увеличением их размера, большим содержанием ферментов, нарастанием способстности к фагоцитозу и уничтожению микробов и опухолевых клеток, может быть и неспецифичной: за счет стимуляции иными (не относящимися к имеющемуся патологическому процессу) микроорганизмами, минеральным маслом, лимфокинами, продуцируемыми Т-лимфоцитами, в меньшей степени — В-лимфоцитами.
Макрофаги активно участвуют в резорбции кости и хряща. При электронномикроскопическом исследовании на границе паннуса и суставного хряща обнаружены макрофаги, тесно связанные с частичками переваренных коллагеновьгх волокон. То же явление отмечено и при контакте макрофагов с резорбируемой костью.
Таким образом, макрофаги играют важную роль в развитии воспалительного процесса, его поддержании и хронизации и уже априорно могут рассматриваться как одна из главных «мишеней» антиревматической терапии.
Опубликовал Константин Моканов
Источник
Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
Одним из первых результатов воспаления является «ограждение» области повреждения от остальных тканей. Тканевые пространства и лимфатические сосуды в воспаленной области блокируются сгустками фибрина, поэтому через небольшой промежуток времени жидкость с трудом протекает через интерстиций. Этот процесс отгораживания задерживает распространение бактерий или токсических продуктов.
Интенсивность воспалительного процесса обычно пропорциональна степени повреждения ткани. Например, когда стафилококки проникают в ткани, они выделяют смертельно опасные клеточные токсины. В результате воспаление развивается быстро, гораздо быстрее, чем сами стафилококки могут размножиться и распространиться. Следовательно, для локальной стафилококковой инфекции характерно быстрое отгораживание, предохраняющее от распространения ее по телу.
Стрептококки, напротив, не вызывают такого интенсивного локального разрушения тканей. Следовательно, процесс отгораживания развивается медленно, на протяжении многих часов, в течение которых стрептококки успевают размножиться и мигрировать. В результате стрептококки часто проявляют гораздо более выраженную тенденцию к распространению в организме и развитию смертельных состояний, чем стафилококки, несмотря на то, что стафилококки гораздо более губительны для тканей.
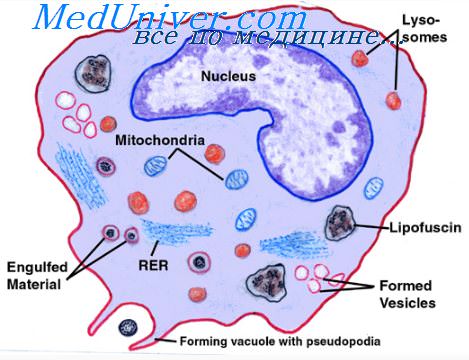
Тканевые макрофаги — первая «линия обороны» против инфекции. В течение нескольких минут после начала воспаления макрофаги, уже присутствующие в тканях, немедленно начинают свое фагоцитарное действие, будь то гистиоциты в подкожных тканях, альвеолярные макрофаги в легких, микроглия в мозге или др. При активации продуктами инфицирования и воспаления первым эффектом является быстрое увеличение каждого из макрофагов.
Затем многие из ранее неподвижных макрофагов отделяются от мест их прикрепления и становятся мобильными, формируя первую «линию обороны» против инфекции в течение примерно первого часа. Количество этих рано мобилизуемых макрофагов часто незначительно, но они спасают жизнь.
Вторжение нейтрофилов в воспаленную область является второй «линией обороны». В течение примерно первого часа после начала воспаления большое число нейтрофилов начинает внедряться в воспаленную область из крови. Этот процесс вызывается продуктами воспаленных тканей, которые инициируют следующие реакции: (1) изменяют внутреннюю поверхность эндотелия капилляров, способствуя прилипанию нейтрофилов к стенкам капилляров в воспаленной области.
Этот эффект, показанный на рисунке, называют маргинацией (или краевым стоянием лейкоцитов), (2) ведут к разрыхлению сцеплений между эндотелиальными клетками капилляров и небольших венул, обеспечивая появление достаточно больших отверстий для прохождения нейтрофилов путем диапедеза непосредственно из крови в тканевые пространства; (3) другие продукты воспаления вызывают хемотаксис нейтрофилов в направлении поврежденных тканей, как объяснялось ранее.
Таким образом, в течение нескольких часов после начала повреждения тканей область обильно заполняется нейтрофилами. Поскольку нейтрофилы крови — уже зрелые клетки, они готовы немедленно начать свои очистительные функции для уничтожения бактерий и удаления инородного материала.
— Также рекомендуем «Нейтрофилия. Защитные механизмы воспаления»
Оглавление темы «Клетки иммунитета. Виды иммунитета»:
1. Ретикулоэндотелиальная система. Макрофаги в лимфатических узлах
2. Альвеолярные макрофаги в легких. Клетки Купфера печени
3. Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
4. Нейтрофилия. Защитные механизмы воспаления
5. Образование гноя. Эозинофилы и базофилы
6. Лейкопения. Лейкемии и его типы
7. Врожденный иммунитет. Приобретенный или адаптивный иммунитет
8. Типы приобретенного иммунитета. Лимфоциты в приобретенном иммунитете
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Роль лимфоцитарных клонов. Происхождение клонов лимфоцитов
Источник

