Системное воспаление при хобл
Традиционно хроническая обструктивная болезнь легких (ХОБЛ) считалась болезнью легких, сопровождающейся хронической бронхиальной обструкцией и прогрессирующими структурными изменениями в дыхательных путях (бронхит) и в паренхиме легких (эмфизема). Была установлена связь структурных изменений с воспалительной реакцией в дыхательных путях, альвеолах и легочных сосудах. Однако воспалительная реакция обнаруживается и в системном кровотоке, что проявляется повышением количества лейкоцитов в крови, уровня острофазовых белков (С-реактивного белка и фибриногена), интерлейкина-6 (ИЛ-6), фактора некроза опухолей (ФНО-α) в сыворотке крови. Многочисленными исследованиями подтверждается, что системное воспаление вносит значительный вклад в патогенез экстрапульмональных проявлений болезни, так называемых системных эффектов. К наиболее значимым системным эффектам хронической обструктивной болезни легких относят потерю массы тела, мышечную дисфункцию, повышенный риск сердечно-сосудистых заболеваний, остеопороз, анемию, депрессию.
Клиническое и прогностическое значение системных эффектов хронической обструктивной болезни легких представлено в Глобальной стратегии диагностики, лечения и профилактики хронической обструктивной болезни легких, пересмотренной в 2007 г. рабочей группой GOLD (Global Initiative for Chronic Obstructive Lung Disease). Таким образом, дефиниция ХОБЛ в настоящее время выглядит следующим образом: хроническая обструктивная болезнь легких — заболевание, которое характеризуется хроническим ограничением скорости воздушного потока, разнообразными патологическими изменениями в легких, существенными внелегочными проявлениями и серьезными сопутствующими заболеваниями, которые могут дополнительно отягощать течение ХОБЛ. Выраженность системных проявлений увеличивается с прогрессированием обструкции, поэтому указанные проявления часто недооцениваются и становятся очевидными на поздних стадиях болезни. Системные проявления снижают качество жизни, способствуют ранней инвалидизации и вносят значительный вклад в смертность больных с ХОБЛ. Одним из наиболее серьезных и социально значимых системных проявлений хронической обструктивной болезни легких является остеопороз.
В настоящее время остеопороз рассматривается как заболевание скелета, при котором снижена прочность кости и повышен риск переломов. В этиопатогенетической классификации остеопороза, принятой на заседании президиума Российской ассоциации по остеопорозу в январе 1997 г., хроническая обструктивная болезнь легких указывается как одна из причин вторичного остеопороза.
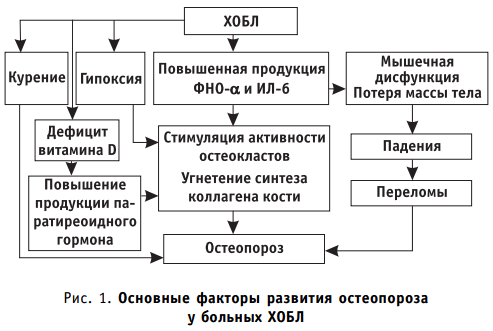
Ведущую роль в патогенезе остеопороза при ХОБЛ играет системное воспаление, которое ассоциировано с продукцией хемоаттрактантов и маркеров воспаления. Результаты научных исследований свидетельствуют о повышении уровня С-реактивного белка, фибриногена, ИЛ-6, ФНО-α, растворимых рецепторов типов 1 и 2 ФНО-α. Предполагается, что провоспалительные цитокины ФНО-α и ИЛ-6 могут стимулировать остеокласты и усиливать резорбцию костной ткани, способствуя тем самым развитию остеопороза. Системное воспаление при ХОБЛ приводит также к усилению катаболизма белков. У пациентов с ХОБЛ происходит снижение количества нежировой ткани и повышение каталитической активности ферментов, приводящее к мышечной дисфункции и потере костной массы. Возможные механизмы развития остеопороза у больных ХОБЛ представлены на рис. 1.

Остеопороз у больных ХОБЛ часто не диагностируется, так как развивается постепенно и в течение долгого времени остается бессимптомным, а внимание врачей обращено на респираторную симптоматику и функциональные показатели. Тем не менее, остеопороз с возможными переломами является важной проблемой для пациентов с ХОБЛ. Переломы сопровождаются болевым синдромом, ограничением физической активности, снижением качества жизни, способствуют ухудшению респираторной функции, являются причиной временной нетрудоспособности, инвалидизации и смертности. Наиболее характерными для остеопороза у больных ХОБЛ являются компрессионные переломы позвоночника (чаще грудного отдела), которые могут приводить к увеличению грудного кифоза и вторично влиять на респираторную функцию. Несмотря на то, что переломы чаще случаются у пациентов с выраженной степенью хронической обструктивной болезни легких, выявление остеопений на начальных стадиях позволяет принять превентивные меры и снизить риск переломов.
Диагностика
«Золотым стандартом» диагностики остеопороза считается двухэнергетическая рентгеновская абсорбциометрия — dual energy X-ray absorptiometry (DXA), так как при небольшой дозе облучения можно исследовать важные в плане остеопороза отделы скелета. Метод основан на измерении степени ослабления костной тканью пучка рентгеновского излучения при линейном сканировании позвонков и шейки бедренной кости. При проведении денситометрии методом DXA оценивается количество минерализованной костной ткани в сканируемой площади (в г/см2); кроме того, полученные результаты сравниваются с референсной базой данных и представляются в виде Т-критерия (количество стандартных отклонений выше или ниже среднего показателя пиковой костной массы молодых женщин) и Z-критерия (количество стандартных отклонений от возрастной нормы). В 1994 г. группой экспертов ВОЗ были сформулированы диагностические критерии остеопороза (табл. 1), которые основаны на количественной оценке минеральной плотности кости различных областей скелета по Т-критерию.
Таблица 1.
Критерии остеопороза (ВОЗ, Женева, 1994)
| Категория | Значения Т-критерия |
| Норма | Более-1 стандартного отклонения |
| Остеопения | От -1 до -2,5 стандартных отклонений |
| Остеопороз | -2,5 стандартных отклонения и ниже |
| Тяжелый остеопороз | -2,5 стандартных отклонения и ниже с наличием в анамнезе 1 и более переломов |
Ультразвуковая денситометрия, в частности, костная ультрасонометрия (КУС) позволяет исследовать только кости периферического скелета. Кроме того, ультразвуковые денситометры не стандартизированы, не определены для них значения Т-критерия, соответствующие остеопении и остеопорозу, поэтому их нельзя рассматривать в качестве инструмента для количественной диагностики снижения минеральной плотности кости (МПК), они не являются альтернативой DXA при скрининге, результаты костной ультрасонометрии не могут служить основанием для назначения лечения остеопороза и контроля за его эффективностью.
При количественной компьютерной томографии производится трехпространственное измерение минеральной плотности кости c определением количества минерализованной костной ткани на объем кости в г/см3, однако в клинической практике метод не нашел широкого распространения.
Рентгенологическое исследование костей скелета в настоящее время рекомендуется использовать только для диагностики переломов костей любой локализации и для дифференциальной диагностики заболеваний скелета, так как рентгенологические признаки остеопороза проявляются только при потере 30-40% костной массы.
При диагностике остеопороза важна также оценка метаболизма костной ткани. Для этого используются показатели фосфорно-кальциевого обмена и биохимические маркеры костного метаболизма. К обязательным методам исследования относят определение в крови уровня общего или ионизированного кальция, фосфора, магния, а также исследование суточной экскреции кальция и фосфора или их исследование в моче натощак по отношению к экскреции креатинина; паратиреоидный гормон и активные метаболиты витамина D определяются по строгим показаниям. Биохимические маркеры костного метаболизма исследуют для оценки скорости процессов костного ремоделирования и выявления разобщенности костной резорбции и костеобразования.
К маркерам костеобразования относят активность общей щелочной фосфатазы в крови и ее костного изофермента, остеокальцин (синтезируемый остеобластами), карбокси- и аминоконцевые пропептиды проколлагена 1 типа.
К маркерам резорбции костной ткани относят экскрецию оксипролина с мочой, активность кислой тартратрезистентной фосфатазы и определение продуктов распада коллагена: пиридинолина, дезоксипиридинолина, N- и C-концевых телопептидов. В настоящее время в Республике Беларусь определяются такие маркеры костного метаболизма, как щелочная фосфатаза, остеокальцин и С-телопептид (β-CTX).
Доказано, что у больных ХОБЛ, получающих ингаляционные глюкокортикостероиды в течение года, выявлялся достоверно более низкий уровень остеокальцина (р < 0,0001), кальция (р < 0,004) и кортизола (р < 0,026) в сыворотке крови, чем в группе контроля. Изучалось также влияние беклометазона и будесонида на костный метаболизм и минеральную плотность кости. При этом выявлено, что оба препарата снижали уровни маркеров костеобразования остеокальцина и С-концевого пропептида проколлагена I типа, но на повышение уровня маркера костной резорбции С-концевого телопептида коллагена I типа и снижение минеральной плотности кости больше влиял беклометазон. Минеральная плотность кости нелеченных больных ХОБЛ отрицательно коррелировала с уровнем С-концевого телопептида коллагена типа I, маркера костной резорбции (r = −0,444; р < 0,001), но не коррелировала с уровнем остеокальцина, маркера костеобразования, что свидетельствует об усилении процессов резорбции у этой группы пациентов.
Одним из наиболее информативных методов диагностики и дифференциальной диагностики остеопороза является биопсия костной ткани из гребня крыла подвздошной кости с последующим гистоморфометрическим исследованием, что позволяет различить остеопороз и другие виды патологии костной ткани, а также охарактеризовать тип обмена в костной ткани.
Лечение и профилактика
В настоящее время не существует руководств по профилактике и лечению остеопороза у больных ХОБЛ. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких не содержит каких-либо рекомендаций по лечению остеопороза у этой группы пациентов. Согласно имеющимся рекомендациям Российской ассоциации по остеопорозу, основными направлениями профилактики остеопороза являются обеспечение полноценного питания с достаточным количеством кальция, фосфора, витаминов и минералов, поддержание физической активности, отказ от вредных привычек (курение, алкоголь), предупреждение падений, фармакопрофилактика, создание образовательных программ.
Применяющиеся для лечения и профилактики остеопороза лекарственные средства по механизму действия подразделяют на препараты, замедляющие костную резорбцию (эстрогены, селективные модуляторы эстрогеновых рецепторов, бисфосфонаты, кальцитонины, кальций), стимулирующие костеобразование (фториды, паратиреоидный гормон, гормон роста, анаболические стероиды, андрогены) и препараты, обладающие многоплановым действием (витамин D и его активные метаболиты, оссеин-гидроксиаппатитный комплекс, соли стронция).
Обязательным компонентом любой схемы профилактики и лечения остеопороза является адекватное употребление кальция и витамина D, содержащихся в пищевых продуктах и лекарственных препаратах.
Известно, что назначение заместительной гормональной терапии женщинам в постменопаузе снижает риск переломов. Выявлено также, что у женщин, принимающих глюкокортикостероиды (ГКС), лечение эстрогенами или прогестероном уменьшает скорость потери минеральной плотности кости. Дефицит тестостерона у мужчин с ХОБЛ, усугубляющийся на фоне лечения системными глюкокортикостероидами, является одним из факторов развития остеопороза у данной категории пациентов. С учетом снижения мышечной массы у больных ХОБЛ и катаболического эффекта глюкокортикостероидов назначение тестостерона может иметь еще и дополнительные показания для увеличения мышечной массы и снижения жировой ткани.
Кальцитонин тормозит резорбцию кости за счет угнетения активности остеокластов, а также обладает анальгетическим эффектом. При применении кальцитонина в большей степени наблюдается улучшение качества кости, чем увеличение показателей минеральной плотности кости, что приводит, тем не менее, к снижению риска вертебральных переломов.
Бисфосфонаты подавляют резорбцию костной ткани, обладают доказанной эффективностью в повышении минеральной плотности кости и снижении риска переломов, могут использоваться для профилактики и лечения различных форм остеопороза. Получены данные, что применение ризедроната предотвращает потерю минеральной плотности кости при длительном применении глюкокортикостероидов. Так, у принимающих плацебо снижение минеральной плотности кости составило 2,8%, а у принимающих 5 мг ризедроната наблюдался прирост минеральной плотности кости (0,6%). Небольшое количество исследований посвящено изучению эффективности лечения остеопороза бисфосфонатами у больных пульмонологического профиля. В исследовании B. J. Smith et al. проводилось изучение влияния алендроната на минеральную плотности кости у больных легочными заболеваниями. У принимавших алендронат/кальций (10 мг / 600 мг в день) в течение 12 месяцев выявлено повышение минеральной плотности кости в поясничном отделе позвоночника по сравнению с принимавшими плацебо/кальций; изменений минеральной плотности кости бедра не наблюдалось.
Стронция ранелат способствует формированию костной ткани и, одновременно, предотвращает резорбцию кости, оказывая двойное действие на костное ремоделирование. Препарат существенно повышает минеральную плотности кости, а также обладает доказанной эффективностью в отношении снижения риска как вертебральных, так и невертебральных переломов.
Заключение
Представленный обзор литературы демонстрирует повышенный риск возникновения остеопороза у пациентов с ХОБЛ. Поэтому при наличии дополнительных факторов риска (низкая масса тела, выраженная дыхательная недостаточность, низкая физическая активность, переломы в анамнезе, прием системных и ингаляционных глюкокортикостероидов) у больных ХОБЛ необходим мониторинг минеральной плотности кости для раннего выявления потери костной массы. Своевременная профилактика и лечение остеопороза позволяют предотвратить переломы, которые снижают качество жизни больных, увеличивают заболеваемость и смертность.
Харевич О. Н., Лаптева И. М., Никитина Л. И., Лаптева Е. А.
Республиканский научно-практический центр пульмонологии и фтизиатрии, Республиканский клинический медицинский центр Управления делами Президента Республики Беларусь.
Журнал «Медицинская панорама» № 9, октябрь 2009.
Источник
Содержание
- Общие сведения
- Диагностика
- Лабораторные и инструментальные исследования
- Лечение
- Профилактика обострений
- Физиотерапия
- Реабилитация
- Медикаментозное лечение
- Профилактика гриппа и пневмококковой пневмонии
- Длительная кислородотерапия
- Записаться на прием
Общие сведения
Хронический бронхит — это заболевание, которое характеризуется следующими признаками: кашлем с мокротой на протяжении по крайней мере трех месяцев в году в течение двух лет подряд в сочетании с нарушениями по данным спирометрии (исследования функции внешнего дыхания).
Таким образом, основная жалоба при хроническом бронхите — это кашель с мокротой.
Вместе с эмфиземой легких хронический бронхит относится к так называемым хроническим обструктивным болезням (заболеваниям) легких, сокращенно — ХОБЛ (или ХОЗЛ). Эмфизема легких характеризуется их «перерастяжением», увеличением воздушных пространств.
Главная жалобы при эмфиземе легких — одышка (чувство нехватки воздуха).
Хронический бронхит и эмфизема легких редко встречаются в чистом виде: у большинства больных в той или иной степени сочетаются оба заболевания. В зависимости от преобладающих симптомов различают два типа ХОБЛ: бронхитический и эмфизематозный.
Основная причина ХОБЛ — курение. У некоторых курильщиков ХОБЛ протекают с приступами удушья. Эту форму заболевания необходимо дифференцировать с бронхиальной астмой, при которой тоже возникают приступы удушья, но между приступами, в отличие от ХОБЛ, проходимость дыхательных путей полностью восстанавливается. Эта форма ХОБЛ получила название хронического астматического бронхита.
В развитых странах ХОБЛ — четвертая по частоте причина смерти. Распространенность ХОБЛ увеличивается с возрастом. Среди больных преобладают мужчины, что закономерно, ведь раньше курение было в основном мужской привычкой. По мере приобщения к ней женщин растет их доля среди больных ХОБЛ.
Главный фактор риска ХОБЛ — курение. Вероятность заболевания увеличивается пропорционально стажу курения и числу выкуриваемых сигарет. У курящих сигары или трубки риск тоже повышен, но в значительно меньшей степени, чем у курящих сигареты. Решающую роль в развитии ХОБЛ, по-видимому, играет индивидуальная восприимчивость к действию табачного дыма, поскольку ХОБЛ развиваются только у 15% курящих.
Больные с недостаточностью альфа1-антитрипсина чрезвычайно предрасположены к эмфиземе легких, правда, на их долю приходится менее 2% случаев этого заболевания. Причиной хронического бронхита могут быть профессиональные вредности, прежде всего контакт с неорганической пылью (цементной, угольной), зерновой пылью и парами серной кислоты. У некурящих развитию ХОБЛ могут способствовать общее загрязнение атмосферы, загрязнение воздуха в помещениях и рецидивирующие инфекции дыхательных путей в детстве, но роль этих факторов не ясна.
Диагностика
Болеют в основном люди старше 50 лет, курящие или курившие ранее (стаж курения — более 20 пачко-лет). Заподозрить ХОБЛ можно при сборе анамнеза, но для подтверждения диагноза необходима спирометрия (исследование функции внешнего дыхания). Основной симптом — прогрессирующая одышка. Обычно ей сопутствуют кашель с мокротой и приступы удушья. Кашель, как правило, либо предшествует одышке, либо появляется одновременно с ней. Мокрота имеет бледно-серый цвет и выделяется по утрам, но может откашливаться и в течение дня.
Многолетний кашель с мокротой и слабо выраженная одышка характерны для бронхитического типа ХОБЛ. При эмфизематозном типе ХОБЛ, напротив, беспокоят редкий кашель со скудной мокротой и выраженная одышка. Изменение характера мокроты со слизистого (бледно-серый цвет) на гнойный свидетельствует о присоединении инфекции — остром бактериальном бронхите. Свистящее дыхание и приступы удушья — результат спазма бронхов или сужения дыхательных путей за счет воспаления. ХОБЛ у близких родственников означает, что причиной заболевания может быть недостаточность альфа1-антитрипсина, особенно если первые симптомы появились до 50 лет. Кровохарканье обычно обусловлено острой бактериальной инфекцией (бронхитом или пневмонией), однако надо исключить рак легкого. Если заболевание началось с прогрессирующей одышки на фоне бронхиальной астмы, особенно у некурящего, вероятен хронический астматический бронхит.
При бронхитическом типе ХОБЛ жалоб в покое обычно нет. Со временем неизбежно развивается гипоксемия (снижение уровня кислорода в крови), которая ведет к изменениям в сердце (легочное сердце) и к сердечной недостаточности (которая проявляется, в частности, отеками).
При ХОБЛ, особенно тяжелых, возможны жалобы, не связанные напрямую с поражением органов дыхания: быстрая утомляемость, похудание, снижение аппетита. Возможны также нарушения сна и психические расстройства: депрессия, нарушения концентрации внимания и памяти.
Лабораторные и инструментальные исследования
Единственный достоверный критерий ХОБЛ — нарушения, выявленные при спирометрии (исследовании функции внешнего дыхания). Любые изменения спирометрических показателей, как в лучшую, так и в худшую сторону, однако, ни о чем не говорят, пока не подтверждены повторными исследованиями. При бронхиальной астме, в отличие от ХОБЛ, обструктивные нарушения обратимы.
Функциональный резерв легких оценивают с помощью нагрузочных проб с исследованием функции внешнего дыхания и газообмена. Кроме того, нагрузочные пробы позволяют установить, чем обусловлена плохая переносимость физической нагрузки: нарушением газообмена или вентиляции либо сердечно-сосудистой патологией. У больных ХОБЛ ограничивающим фактором часто оказывается сердечно-сосудистая патология.
Если выявлены обструктивные нарушения, спирометрию обычно дополняют определением чувствительности к бронходилататорам: для этого дают пациенту сделать несколько вдохов через ингалятор и повторяют исследование. Однако реакция на однократное применение бронходилататоров не всегда отражает их эффективность, и низкая чувствительность к бронходилататорам при спирометрии еще не означает, что длительное их применение не улучшит состояние больного. Следовательно, независимо от реакции, выявленной при спирометрии, не стоит отказываться от пробного лечения бронходилататорами.
Рентгенография грудной клетки может помочь в диагностике эмфиземы легких. Наиболее важный ее признак — перераздувание легких. Можно обнаружить буллы в верхних долях и очаговое повышение прозрачности легочных полей. Рентгенография лишь приблизительно характеризует тяжесть эмфиземы легких и наиболее информативна при тяжелых формах заболевания. В выявлении таких изменений, как мелкие буллы, гораздо большей чувствительностью обладает компьютерная томография (КТ). Однако ни рентгенография, ни КТ не заменяют ключевого метода диагностики — спирометрии.
При первичном обследовании целесообразны также микроскопия мокроты, общий анализ крови с определением лейкоцитарной формулы, электрокардиография (ЭКГ) и часто — эхокардиография (ультразвуковое исследование сердца). Кроме того, при подозрении на недостаточность альфа1-антитрипсина определяют его уровень в сыворотке, а при подозрении на хронический астматический бронхит проводят кожные пробы с аллергенами и определяют уровень IgE в сыворотке.
Лечение
Отказ от курения
Большинство больных ХОБЛ (85%) курят или курили ранее. Отказ от курения не только замедляет скорость снижения показателей внешнего дыхания (она становится такой же, как у некурящего), но и благоприятно сказывается на состоянии сердечно-сосудистой системы и снижает риск рака легкого. С включением в комплексные программы борьбы с курением препаратов никотина (жевательной резинки с никотином, пластыря с никотином, аэрозоля с никотином для интраназального введения, ингалятора с никотином) частота стойкого воздержания от курения достигла 50%. С помощью жевательной резинки в плазме и тканях поддерживается примерно такой же уровень никотина, как при выкуривании пачки сигарет в день. Отменять лечение можно как постепенно, так и резко. Из недостатков следует отметить горький вкус жевательной резинки, что может привести к несоблюдению предписаний врача, и недостаточное поступление никотина в организм при низкой эффективности жевания.
Курению способствуют многие факторы: привычка, влияние окружающих, зависимость. Следовательно, для достижения хороших отдаленных результатов, помимо препаратов никотина в программе борьбы с курением должны быть учтены и эти стороны. Важную роль играют помощь и участие врача.
Профилактика обострений
Обострение ХОБЛ, прежде всего хронического астматического бронхита, нередко вызывают загрязнители воздуха на рабочем месте или в быту. Выявив и устранив их, можно снизить частоту и тяжесть обострений. Обострение ХОБЛ может вызвать сильный смог.
Физиотерапия
Удаление мокроты из дыхательных путей может заметно улучшить самочувствие больного, особенно при бронхитическом типе ХОБЛ. Существует множество способов очищения дыхательных путей от мокроты и предотвращения ее накопления. Кашель у больных ХОБЛ, как правило, не обеспечивает удаление мокроты и лишь изматывает. Таким больным можно посоветовать простой и эффективный способ откашливания мокроты, которым, к сожалению, часто пренебрегают. Суть его заключается в следующем: после пары медленных глубоких вдохов надо задержать дыхание на 5—10 с для повышения внутригрудного давления и затем, на выдохе, откашляться с открытой голосовой щелью.
Постуральный дренаж, вибрационный и перкуссионный массаж облегчают выведение мокроты из нижних отделов легких благодаря действию силы тяжести и колебательным движениям грудной клетки, сообщаемым ей при перкуссии или с помощью вибратора. По завершении процедуры больной должен хорошо откашляться, как описано выше.
Все описанные методы тем или иным образом облегчают удаление мокроты, но переместить мокроту в трахею и крупные бронхи, откуда она может быть удалена при кашле или с помощью аспирации, по-прежнему может только кашель с открытой голосовой щелью.
Реабилитация
ХОБЛ существенно ухудшают качество жизни. В комплексные программы реабилитации входят обучение больных, физические упражнения и восстановление тренированности, надлежащее питание, психотерапия и социальная адаптация для устранения тревожности и других эмоциональных расстройств, вызванных ХОБЛ.
Медикаментозное лечение
Медикаментозное лечение эмфиземы легких и хронического бронхита направлено на ослабление симптомов заболевания и улучшение показателей функции легких. Предпочтение отдается ингаляционным препаратам в виде дозированных аэрозолей, поскольку при введении препарата непосредственно в дыхательные пути риск системных побочных эффектов меньше. Для введения ингаляционных препаратов необходима буферная насадка (спейсер). Она играет роль резервуара для аэрозоля и избавляет от необходимости согласовывать по времени вдох и нажатие на ингалятор-дозатор. Буферная насадка позволяет глубже ввести препарат в дыхательные пути, препятствует его оседанию в ротоглотке.
Основные группы лекарственных средств, используемых при ХОБЛ — это M-холиноблокаторы (ипратропия бромид). Ипратропия бромид обладает более сильным, чем бета-адреностимуляторы или теофиллин, расширяющим действием на бронхи, а также более продолжительным действием. Все это ставит его во главу угла лечения ХОБЛ. Если в обычной дозе (по 2 вдоха 4 раза в сутки) ипратропия бромид недостаточно эффективен, дозу можно безбоязненно увеличить до 3—6 вдохов 4 раза в сутки.
Бета-адреностимуляторы улучшают проходимость дыхательных путей, облегчают отхождение мокроты и ослабляют одышку. Для усиления бронходилатирующего эффекта можно увеличить дозу с 2 вдохов 4 раза в сутки до 2—6 вдохов 4—6 раз в сутки, не опасаясь осложнений. Однако под влиянием сообщений о гибели больных бронхиальной астмой в связи с передозировкой бета-адреностимуляторов специалисты не приветствуют повышение дозы.
Роль глюкокортикоидов для приема внутрь в лечении ХОБЛ остается неопределенной отчасти из-за отсутствия доводов в пользу их применения и тяжелых побочных эффектов. Глюкокортикоиды для приема внутрь показаны амбулаторным больным при недостаточной эффективности бета-адреностимуляторов, ипратропия бромида и, возможно, теофиллина. При длительном применении глюкокортикоиды для приема внутрь оказывают тяжелые побочные действия. Среди них надпочечниковая недостаточность, остеопороз, артериальная гипертония, катаракта, миопатия, сахарный диабет.
Несмотря на то что обоснований для применения ингаляционных глюкокортикоидов при ХОБЛ недостаточно, эти препараты применяют часто. Они содержат меньшие дозы, чем препараты для приема внутрь, почти не всасываются и поэтому вызывают лишь легкие осложнения.
Польза от муколитических и отхаркивающих средств при хроническом бронхите пока под вопросом. Считается, что муколитические средства, например йодированный глицерин и ацетилцистеин, уменьшают вязкость мокроты. Отхаркивающие препараты разжижают мокроту и способствуют ее выведению.
Инфекции провоцируют обострения ХОБЛ, поэтому антибактериальные препараты назначают часто — как с профилактической, так и с лечебной целью. Во время инфекционных обострений (на них указывают усиление одышки и кашля и появление гнойной мокроты) функция легких ухудшается (не исключено, что необратимо). При частых обострениях (4 и более в год) сократить их число может ежемесячная профилактическая антибактериальная терапия в течение недели со сменой препаратов.
Профилактика гриппа и пневмококковой пневмонии
Поскольку легочная инфекция у больных ХОБЛ встречается часто и грозит ухудшением функции легких и дыхательной недостаточностью, больным, не страдающим аллергией на яичный белок, рекомендуется ежегодная вакцинация против гриппа. Эффективность ее достигает 60—80%. Невакцинированным больным с высоким риском гриппа A и на ранней его стадии назначают амантадин. Больным старше 50 лет, кроме того, рекомендуется однократная иммунизация пневмококковой вакциной. Ревакцинацию сейчас проводят по прошествии пяти и более лет, если на момент вакцинации возраст больного не превышал 65 лет.
Длительная кислородотерапия
Польза постоянных ингаляций кислорода (длительной кислородотерапии) при ХОБЛ научно доказана. Кислородотерапия существенно снижает частоту осложнений и летальных исходов при тяжелых ХОБЛ, а также улучшает психические функции и переносимость физической нагрузки.
Источник

