Расстройства микроциркуляции при воспалении
Стадии расстройства микроциркуляции:
1. Кратковременный спазм артериол:результат рефлекторного возбуждения
вазоконстрикторов на воздействие
флогогена (несколько сек–мин).
2. Артериальная гиперемия:увеличение
притока артериальной крови и кровенаполнения
ткани. Способствует усилению оксигенации
тканей, снижению степени ацидоза,
активации обмена веществ.
3. Венозная гиперемия:сопровождается
замедлением тока крови, расширением
просвета посткапилляров и венул. В
механизме выделяют 3 группы факторов:
нарушения реологических свойств крови;
изменения сосудистой стенки;
тканевые изменения.
4. Предстаз:периодические
маятникообразные движения крови «вперёд
↔ назад» в результате механического
препятствия оттоку крови по посткапиллярам,
венулам и венам агрегатами форменных
элементов крови в просвете сосуда и
пристеночными микротромбами.
5. Стаз:возникает в результате
закрытия просвета микрососудов агрегатами
клеток изнутри и сдавления экссудатом
снаружи. Является завершающей стадией
сосудистых изменений.
Экссудация
Экссудация (от лат.exsudatio— выпотевание) — компонент воспаления,
включающий в себя триаду: сосудистые
реакции и изменения кровообращения в
очаге воспаления; выход жидкой части
крови из сосуда (собственно экссудацию);
эмиграцию (выход лейкоцитов в очаг
воспаления и развитие фагоцитарной
реакции).
Основная причинаэкссудации —
увеличение проницаемости стенок
микрососудов вследствие множества
процессов, повреждающих их стенку.

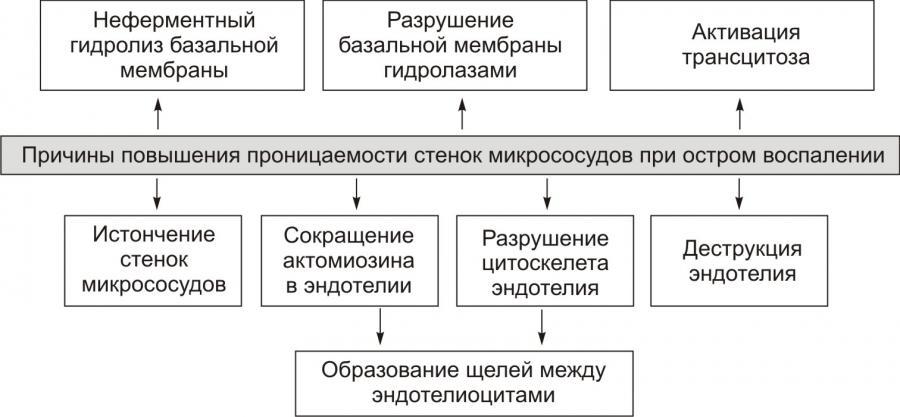
Рис. 9. —
Причины повышения проницаемости стенок
микрососудов
при остром воспалении (по
П.Ф. Литвицкому, 2002)
Основные факторы механизма экссудации:
1) повышение проницаемости сосудов
(венул и капилляров) в результате
воздействия медиаторов воспаления и в
ряде случаев самого воспалительного
агента — ведущий фактор;
2) увеличение кровяного (фильтрационного)
давления в сосудах очага воспаления
вследствие гиперемии;
3) возрастание осмотического и онкотического
давления в воспаленной ткани в результате
альтерации и начавшейся экссудации и,
возможно, снижение онкотического
давления крови из-за потери белков при
обильной экссудации.
Виды экссудата
1. Серозный экссудат: состоит из
полупрозрачной жидкости, богатой белком
(до 2–3%), и немногочисленных клеток, в
том числе форменных элементов крови
(ФЭК).
2. Фибринозный экссудат: содержит
большое количество фибриногена и
фибрина.
3. Гнойный экссудат:мутная густая
жидкость, содержащая до 6–8% белка и
большое количество различных форм
лейкоцитов, микроорганизмов, погибших
клеток повреждённой ткани.
4. Геморрагический экссудат:содержит
большое количество белка и эритроцитов,
а также другие ФЭК.
5. Гнилостный (ихорозный) экссудат:
любой вид экссудата может приобрести
гнилостный (ихорозный) характер при
внедрении в очаг воспаления гнилостной
микрофлоры (анаэробы).
6. Смешанные формыэкссудата могут
быть самыми разнообразными (например,
серозно-фибринозный, гнойно-фибринозный,
гнойно-геморрагический и др.).
Значение процесса экссудации в очаге воспаления
Адаптивное:
транспорт медиаторов воспаления
доставка иммуноглобулинов в очаг
воспаленияудаление из крови метаболитов и токсинов
задержка и/или фиксация в очаге воспаления
флогогена и продуктов его действия на
ткань
Патогенное:
сдавление, смещение органов и тканей
экссудатомвозможность излияния экссудата в
полости тела и сосудыформирование абсцессов, развитие
флегмон
Эмиграция (emigratio, от лат.emigrare
— выселяться, переселяться) — выход
лейкоцитов из сосудов в ткань.Осуществляется путем диапедеза через
стенку венул и является ключевым событием
патогенеза воспаления.
Стадии процесса эмиграции лейкоцитов
в очаге воспаления:
1. краевое стояние лейкоцитов;
2. адгезия к эндотелию и проникновения
через сосудистую стенку;
3. направленное движение лейкоцитов в
очаге воспаления.
На стадии краевого стояния(маргинации)
условно выделено четыре последовательных
этапа.
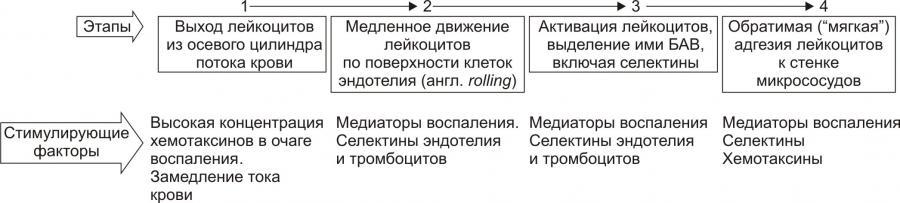
Рис. 10. —Этапы стадии краевого
стояния лейкоцитов и факторы, стимулирующие
краевое стояние (по П.Ф. Литвицкому,
2002)
В стадии адгезии и выхода лейкоцитов
выделяют 2 этапа: устойчивой («плотной»)
адгезии (1) и прохождения лейкоцитов
через стенку микрососуда (2).

Рис. 11. —Этапы стадии устойчивой
адгезии и прохождения лейкоцитов через
стенку микрососуда; факторы, стимулирующие
адгезию (по П.Ф. Литвицкому, 2002)
Значение эмиграции лейкоцитов
в очаг воспаления:
поглощение и деструкция
флогогенного фактора;поглощение и деструкция
поврежденных клеток и неклеточных
структур;синтез и выделение медиаторов воспаления;
поглощение и «процессинг» антигенов
и презентация последних лимфоцитам;развитие иммунных и/или аллергических
реакций.
Источник
Нарушение микроциркуляции в очаге воспаления характеризуется изменением тонуса микроциркуляторных сосудов, усиленным током жидкой части крови за пределы сосуда (т.е. экссудацией) и выходом форменных элементов крови (т.е. эмиграцией).
Для сосудистой реакции характерны 4 стадии:
1) кратковременный спазм сосудов,
2) артериальная гиперемия,
3) венозная гиперемия,
4) стаз.
Спазм сосудов возникает при действии повреждающего агента на ткани и связан с тем, что вазоконстрикторы возбуждаются первыми, поскольку они чувствительнее вазодилятаторов. Спазм длится до 40 секунд и быстро сменяется артериальной гиперемией. Артериальная гиперемия формируется следующими тремя путями: а) как результат паралича вазоконстрикторов; б) как результат воздействия медиаторов с сосудорасширяющей активностью; в) как результат реализации аксон-рефлекса.
Расслабляются прекапиллярные сфинктеры, увеличивается число функционирующих капилляров и кровоток через сосуды поврежденного участка может в десятки раз превышать таковой неповрежденной ткани.
Расширение микроциркуляторных сосудов, увеличение количества функционирующих капилляров и повышенное кровенаполнение органа определяет первый макроскопический признак воспаления — покраснение. Если воспаление развивается в коже, температура которой ниже температуры притекающей крови, то температура воспаленного участка повышается — возникает жар. Поскольку в первое время после повреждения линейная и объемная скорость кровотока в участке воспаления достаточно велики, то оттекающая из очага воспаления кровь содержит большее количество кислорода и меньшее количество восстановленного гемоглобина и поэтому имеет яркокрасную окраску. Артериальная гиперемия при воспалении сохраняется недолго (от 15 минут до часа) и всегда переходит в венозную гиперемию, при которой увеличенное кровенаполнение органа сочетается с замедлением и даже полным прекращением капиллярного кровотока.
Венозная гиперемия начинается с максимального расширения прекапиллярных сфинктеров, которые становятся нечувствительными к вазоконстрикторным стимулам и венозный отток затрудняется. После этого замедляется ток крови в капиллярах и приносящих артериолах. Главной причиной развития венозной гиперемии является экссудация — выход жидкой части крови из микроциркуляторного русла в окружающую ткань. Экссудация сопровождается повышением вязкости крови, периферическое сопротивление кровотоку возрастает, скорость тока крови падает. Кроме того, экссудат сдавливает венозные сосуды, что затрудняет венозный отток и также усиливает венозную гиперемию. Развитию венозной гиперемии способствует набухание в кислой среде форменных элементов крови, сгущение крови, нарушение десмосом, краевое стояние лейкоцитов, образование микротромбов. Кровоток постепенно замедляется и приобретает новые качественные особенности из-за повышения гидростатического давления в сосудах: кровь начинает двигаться толчкообразно, когда в момент систолы сердца кровь продвигается вперед, а в момент диастолы кровь останавливается. При дальнейшем повышении гидростатического давления кровь в систолу продвигается вперед, а в момент диастолы возвращается обратно — т.е.возникает маятникообразное движение. Толчкообразное и маятникообразное движение крови определяет возникновение пульсирующей боли. Постепенно экссудация вызывает развитие стаза — обычное явление при воспалении. Как правило, стаз возникает в отдельных сосудах венозной части микроциркуляторного русла из-за резкого повышения ее проницаемости. При этом жидкая часть крови быстро переходит во внесосудистое пространство и сосуд остается заполненным массой плотноприлежащих друг к другу форменных элементов крови. Высокая вязкость такой массы делает невозможным продвижение ее по сосудам и возникает стаз. Эритроциты образуют «монетные столбики», границы между ними постепенно стираются и образуется сплошная масса в просвете сосуда — сладж (от англ. sludge — тина, грязь).
Источник
Итак, альтерация тканей и последующее выделение медиаторов являются первой стадией воспаления. Уже на этой стадии очень быстро возникают нарушения местного крово- и лимфообращения, прежде всего со стороны микроциркуляторного русла. Реакция со стороны микроциркуляторного русла играет очень большую роль в патогенезе воспаления. Многие авторы утверждают, что весь «облик воспаления», все его особенности определяются в значительной степени реакцией микроциркуляторного русла, степенью изменения проницаемости сосудов и глубиной их поражения.
Воспаление характеризуется определенной динамикой изменения кровообращения, последовательностью сосудистых реакций (рис. 5.1).
Сначала происходит кратковременный спазм артериол. По данным некоторых авторов, он может длиться от 10—20 с до нескольких минут. Спазм возникает в результате непосредственного воздействия повреждающего агента на сосуды, что приводит к освобождению из поврежденных эндотелиальных клеток и тромбоцитов сосудосуживающих веществ — катехоламинов, лейкотриенов, эндотелинов. В развитии спазма может принимать участие рефлекторное повышение тонуса вазоконстрикторов. Спазм артериол — необязательная реакция, он возникает лишь в тех случаях, когда раздражитель, вызывающий воспаление, действует быстро и сильно.

Рис. 5.1. Изменение кровообращения в очаге воспаления:
1 — спазм сосудов; 2 — артериальная гиперемия (расширение капилляров, увеличение количества функционирующих капилляров); 3 — венозная гиперемия (усиление фильтрации)
Очень быстро спазм сосудов сменяется артериальной гиперемией, когда имеют место расширение артериол и капилляров, увеличение количества функционирующих капилляров, увеличение линейной и объемной скорости кровотока, повышение внутрикапиллярного давления и некоторое усиление процессов фильтрации. В основе развития воспалительной артериальной гиперемии лежат следующие механизмы:
- 1) рефлекторный — активация аксон-рефлекса, местного сосудорасширяющего рефлекса, который реализуется при раздражении чувствительных волокон, участвующих в восприятии боли и высвобождающих при этом сосудорасширяющие пептиды;
- 2) нейропаралитический (в силу пареза вазоконстрикторов в кислой среде происходит инактивация действия катехоламинов);
- 3) миопаралитический (за счет снижения базального тонуса сосудов). Падение базального тонуса обусловлено действием накапливающихся вазоактивных медиаторов воспаления и ионов водорода, которые расслабляют мышечные элементы стенки артериол и прекапилляров. Этот механизм является основным в развитии воспалительной артериальной гиперемии;
- 4) разрушение соединительной ткани вокруг сосудов. Жесткость капилляров в значительной мере (до 93%) определяется окружающей соединительной тканью. Распад соединительной ткани приводит к снижению механического противодействия растягивающему усилию давления крови внутри сосуда.
Активная артериальная гиперемия может продолжаться в течение нескольких часов и суток. Многие внешние признаки воспаления связаны как раз с развитием артериальной гиперемии.
Необходимо отметить одну особенность воспалительной артериальной гиперемии, отличающую ее от гиперемии невоспалительного характера. Эта особенность состоит в том, что капиллярная дилатация при воспалении носит первичный характер, она зависит не столько от притока крови по приносящим артериям, сколько от локальных изменений, происходящих в очаге воспаления. При этом капиллярная дилатация при воспалении более выражена.
По мере нарастания воспалительного процесса артериальная гиперемия сменяется венозной. Венозная гиперемия характеризуется замедлением кровотока, преимущественным расширением капилляров и венул, повышением в них гидростатического давления, резким усилением процессов фильтрации, нарушением реологических свойств крови, феноменом краевого стояния лейкоцитов и их эмиграцией. Факторы, влияющие на переход артериальной гиперемии в венозную, можно разделить на две группы: внутрисосудистые и вне- сосудистые. К внутрисосудистым факторам относятся сгущение крови вследствие перехода части плазмы из крови в воспаленную ткань, набухание эндотелия в кислой среде, пристеночное стояние лейкоцитов, образование микротромбов вследствие агрегации тромбоцитов и увеличения свертываемости крови, снижение сосудистого тонуса. Внесосудистые факторы — это избыточное накопление в очаге воспаления медиаторов воспаления с сосудорасширяющим действием, ионов водорода, сдавление экссудатом стенок вен и лимфатических сосудов, снижение упругости соединительной ткани.
Венозная гиперемия первоначально приводит к развитию престаза — толчкообразному, маятникообразному движению крови «вперед — назад». Во время систолы кровь движется от артерии к венам, во время диастолы — в противоположном направлении, так как кровь встречает препятствие к оттоку по венулам в виде возросшего в них кровяного давления. И наконец, движение крови из-за закупорки сосудов агрегатами клеток или микротромбами полностью прекращается, развивается стаз.
Благодаря венозной гиперемии и стазу в значительной степени ограничивается распространение патогенного агента, и воспаление, таким образом, выполняет свою защитную барьерную функцию.
Источник
Воспаление характеризуется нарушением местного крово- и лимфообращения, прежде всего микроциркуляции. Микроциркуляцией принято называть движение крови в терминальном сосудистом русле (в артериолах, метартериолах, капиллярных сосудах и венулах), а также транспорт различных веществ через стенку этих сосудов.
В Фазу экссудации происходит изменения в мцр.
Динамика сосудистых реакций и изменения в очаге кровообращения при развитии воспаления стереотипны:
1. Вначале воспалительного процесса возникает кратковременных рефлекторный спазм артериол и прекапилляров, который скоро проходит Наблюдать этот феномен можно по замедлению кровотока.
2. Затем, сменяя друг друга, развиваются артериальная и венозная гиперемия.
· Артериальная гиперемия — является результатом образования в воспаленном очаге большого количества вазоактивных веществ — медиаторов воспаления, которые расслабляют мышечные элементы стенки артериол и прекапилляров. Это приводит к увеличению притока артериальной крови, ускоряет ее движение, открывает ранее не функционировавшие капилляры, повышает в них давление. Кроме того, приводящие сосуды расширяются в результате паралича вазоконстрикторов, сдвига рН среды в сторону ацидоза, накопления ионов калия(гиперкалийионии)
· Венозная гиперемия — скорость движения крови уменьшается, меняется характер кровотока. Так, если при артериальной гиперемии клетки крови располагались в центре сосуда (осевой ток), а у стенок находились плазма и небольшое число лейкоцитов (плазматический ток), то теперь такое разделение нарушается. Изменяются реологические свойства крови. Она становится более густой и вязкой, эритроциты набухают, образуя агрегаты, т.е. беспорядочные скопления, которые медленно движутся или совсем останавливаются в сосудах малого диаметра.
Развитие венозной гиперемии объясняется действием ряда факторов, которые можно разделить на три группы:
1 факторы крови,
2 факторы сосудистой стенки,
3 факторы окружающих тканей.
· Факторы крови: краевое расположение лейкоцитов, набухание эритроцитов, выход жидкой части крови в воспаленную ткань и сгущение крови, образование тромбов вследствие активации фактора Хагемана, уменьшения содержания гепарина.
· Факторы сосудистой стенки: Влияние факторов сосудистой стенки на венозную гиперемию проявляется набуханием эндотелия, в результате чего просвет мелких сосудов еще больше сужается. Измененные венулы теряют эластичность и становятся более податливыми сдавливающему действию инфильтрата.
· Факторы окруж тканей: отечная ткань, сдавливая вены и лимфатические сосуды, способствует развитию венозной гиперемии.
3. И, наконец, развивается престаз (толчкообразный кровоток, маятникообразное движение крови) и стаз — остановка кровотока. В результате стаза формируется своеобразный барьер, обеспечивающий ограничительную функцию очага воспаления
Благодаря экссудации происходит отграничение очага воспаления, разбавление токсинов и продуктов распада тканей, осуществляется защита от флогогенных агентов и поврежденных клеток с помощью ферментов и иммуноглобулинов.
Механизмы экссудации и формирования воспалительного отека. Биологическая роль воспалительного отека. Виды экссудатов.
Выход жидкой части крови в очаг воспаления (собственно экссудация) происходит вследствие резкого усиления процесса фильтрации, а накопление жидкости в тканях связано со снижением процесса резорбции из-за увеличения венозного давления.
Экссудация определяется прежде всего
· увеличением кровяного (фильтрационного) давления в венозной части капилляров воспаленной ткани.
· повышение проницаемости капиллярной стенки .
Основной причиной экссудации является повышение проницаемости гистогематического барьера, т. е. сосудистой стенки, прежде всего капиллярных сосудов и венул. выход жидкости и растворенных в ней веществ осуществляется в местах соприкосновения эндотелиальных клеток. Щели между ними могут увеличиваться при расширении сосудов, а также при округлении эндотелиальных клеток. Кроме того, клетки эндотелия способны «заглатывать» мельчайшие капельки жидкости (микропиноцитоз), переправлять их на противоположный конец клетки и выбрасывать в близлежащую среду (экструзия).
В связи с выходом белка из сосудистого русла, его количество вне сосудов увеличивается, что способствует повышению онкотического давления в тканях. Гиперонкия и гиперосмия в очаге альтерации создают приток жидкости в воспаленную ткань.
Экссудат как воспалительная жидкость в отличие от транссудата содержит большое количество белка, ферментов, иммуноглобулинов, клеток крови и остатки тканевых элементов (клеточный детрит). Благодаря экссудации происходит отграничение очага воспаления, разбавление токсинов и продуктов распада тканей, осуществляется защита от флогогенных агентов и поврежденных клеток с помощью ферментов и иммуноглобулинов.
Источник
