Пролиферация при воспалении обеспечивает
2.1.10. Механизмы развития пролиферации в очаге воспаления
Пролиферация является завершающей фазой развития воспаления, обес-печивающей репаративную регенерацию тканей на месте очага аль-
терации. Пролиферация развивается с самого начала воспаления наряду с яв-лениями альтерации и экссудации.
При репаративных процессах в очаге воспаления регенерация клеток и фиброплазия достигаются как активацией процессов пролиферации, так и ог-раничением апоптоза клеток. Размножение клеточных элементов начинается по периферии зоны воспаления, в то время как в центре очага могут еще про-грессировать явления альтерации и некроза. Полного развития пролиферация соединительнотканных и органоспецифических клеточных элементов дости-гает после «очистки» зоны повреждения от клеточного детрита и инфекци-онных возбудителей воспаления тканевыми макрофагами и нейтрофилами. В связи с этим следует отметить, что процессу пролиферации предшествует формирование нейтрофильного и моноцитарного барьеров, которые форми-руются по периферии зоны альтерации.
Восстановление и замещение поврежденных тканей начинается с выхода из сосудов молекул фибриногена и образования фибрина, который формиру-ет своеобразную сетку, каркас для последующего клеточного размножения. Уже по этому каркасу распределяются в очаге репарации быстро образую-щиеся фибробласты. Деление, рост и перемещение фибробластов возможны только после их связывания с фибрином или коллагеновыми волокнами. Эта связь обеспечивается особым белком – фибронектином. Размножение фиб-робластов начинается по периферии зоны воспаления, обеспечивая формиро-вание фибробластического барьера. Хемотаксис, активация и пролиферация фибробластов осуществляются под воздействием:
1. Факторов роста фибробластов.
2. Тромбоцитарного фактора роста.
3. Цитокинов — ФНО, ИЛ-1.
4. Кининов.
5. Тромбина.
6. Трансформирующего фактора роста b.
Сначала фибробласты не зрелые и не обладают достаточной синтетиче-ской активностью. Созреванию предшествует внутренняя структурно-функциональная перестройка фибробластов: гипертрофия ядра и ядрышка, гиперплазия ЭПС, повышение содержания ферментов, особенно щелочной фосфатазы, неспецифической эстеразы, b-глюкуронидазы. Только после пе-рестройки фибробласты начинают синтезировать коллаген, эластин, коллаге-нассоциированные белки и протеогликаны. Коллагеногенез стимулируется следующими биологически активными веществами — ФНО, ИЛ-1, ИЛ-4, фак-тором роста фибробластов, тромбоцитарным фактором роста.
Интенсивно размножающиеся фибробласты продуцируют кислые муко-полисахариды – основной компонент межклеточного вещества соединитель-ной ткани (гиалуроновую кислоту, хондроитинсерную кислоту, глюкозамин, галактозамин). При этом зона воспаления не только инкапсулируется, но и начинаются постепенная миграция клеточных и бесклеточных компонентов соединительной ткани от периферии к центру, формирование соединитель-нотканного остова на месте первичной и вторичной альтерации.
Наряду с фибробластами размножаются и другие тканевые и гематоген-ные клетки. При разрушении базальных мембран сосудов в зоне альтерации происходит миграция клеток эндотелия по градиенту ангиогенных факторов. Просвет новообразующегося капилляра формируется путем слияния внекле-точных пространств соседних эндотелиоцитов. Вокруг новообразующихся капилляров концентрируются тучные клетки, макрофаги, нейтрофилы, кото-рые освобождают биологически активные вещества, способствующие про-лиферации капилляров.
Важнейшими факторами, стимулирующими ангиогенез, являются:
1. Факторы роста фибробластов (основной и кислый).
2. Сосудистый эндотелиальный фактор роста.
3. Трансформирующие факторы роста .
4. Эпидермальный фактор роста.
Фибробласты вместе с вновь образованными сосудами создают грануля-ционную ткань. Это, по существу, молодая соединительная ткань, богатая клетками и тонкостенными капиллярами, петли которых выступают над по-верхностью ткани в виде гранул.
Основными функциями грануляционной ткани являются: защитная – пре-дотвращение влияния факторов окружающей среды на очаг воспаления и ре-паративная – заполнение дефекта и восстановление анатомической и функ-циональной полноценности поврежденных тканей.
Формирование грануляционной ткани не строго обязательно. Это зависит от величины и глубины повреждения. Грануляционная ткань обычно не раз-вивается при заживлении ушибленных кожных ранок или мелких поврежде-ний слизистой оболочки (Кузин М.И., Костюченок Б.М. и соавт., 1990). Гра-нуляционная ткань постепенно превращается в волокнистую ткань, называе-мую рубцом. В рубцовой ткани уменьшается количество сосудов, они запус-тевают, уменьшается количество макрофагов, тучных клеток, снижается ак-тивность фибробластов. Небольшая часть клеточных элементов, распола-гающаяся среди коллагеновых нитей, сохраняет активность. Предполагают, что сохранившие активность тканевые макрофаги принимают участие в рас-сасывании рубцовой ткани и обеспечивают формирование более мягких руб-цов.
Параллельно с созреванием грануляций происходит эпителизация раны. Она начинается в первые часы после повреждения, и уже в течение первых суток образуются 2-4 слоя клеток базального эпителия. Скорость эпителиза-ции обеспечивается следующими процессами: миграцией, делением и диф-ференцировкой клеток. Эпителизация небольших ран осуществляется, в ос-новном, за счет миграции клеток из базального слоя. Раны более крупные эпителизируются за счет миграции и митотического деления клеток базаль-ного слоя, а также дифференцировки регенерирующего эпидермиса. Новый эпителий образует границу между поврежденным и подлежащим слоем, он препятствует обезвоживанию тканей раны, уменьшению в ней электролитов и белков, а также предупреждает инвазию микроорганизмов.
В процессе пролиферации участвуют и органспецифические клеточные элементы органов и тканей. С точки зрения возможностей пролиферации ор-ганспецифических клеточных элементов все органы и ткани могут быть рас-классифицированы на три группы:
К первой группе могут быть отнесены органы и ткани, клеточные элемен-ты которых обладают активной или практически неограниченной пролифе-рацией, достаточной для полного восполнения дефекта структуры в зоне воспаления (эпителий кожи, слизистых оболочек дыхательных путей, слизи-стой желудочно-кишечного тракта, мочеполовой системы; гемопоэтическая ткань и др.).
Ко второй группе относятся ткани с ограниченными регенерационными способностями (сухожилия, хрящи, связки, костная ткань, периферические нервные волокна).
К третьей группе относятся те органы и ткани, где органоспецифические клеточные элементы не способны к пролиферации (сердечная мышца, клетки ЦНС). Основными факторами, регулирующими процессы пролиферации и дифференцировки клеток в очаге воспаления, являются:
1. Факторы роста, продуцируемые макрофагами, лимфоцитами, тромбо-цитами, фибробластами и другими клетками, стимулированными в зоне вос-паления. К ним относятся:
— факторы роста эпидермиса (стимулятор пролиферации и созрева-ния эпителия, стимулятор ангиогенеза);
— трансформирующий фактор роста- (стимулятор ангиогенеза);
— трансформирующий фактор роста- (хемоаттрактант фибробла-стов, стимулятор синтеза коллагена, фибронектина, ангиогенеза, ингибитор протеолиза);
— тромбоцитарный фактор роста (стимулятор миграции, пролифе-рации и синтеза белка в клетках-мишенях, обладает провоспалительным эф-фектом);
— фактор роста эндотелиоцитов;
— фактор роста фибробластов кислый и основной (стимуляторы пролиферации всех клеток сосудистой стенки);
— колониестимулирующие факторы (гранулоцитарный и макрофа-гальный стимуляторы дифференцировки, пролиферации и функциональной активности клеток гранулоцитарного и моноцитарного ряда) — цитокины (ФНО, ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7) , продуцируемые Т- и В-лимфоцитами, мононуклеарами, тучными клетками, фибробластами, эндоте-лиоцитами, обеспечивают хемотаксис, фиброгенез, ингибируют апоптоз, стимулируют процессы пролиферации в очаге воспаления. Ингибиторами роста для некоторых клеток служат те же цитокины, которые стимулируют пролиферацию других – это ФНО, трансформирующий фактор роста и - интерферон (Зайчик А.Ш., Чурилов Л.П., 1999);
— фактор роста нервов (стимулятор пролиферации, роста, морфоге-неза симпатических нейронов, эпителиальных клеток). Ростовые факторы, взаимодействуя с рецепторами на клетках- мишенях, могут непосредственно стимулировать синтез ДНК в клетках или подготавливать внутриклеточные рецепторы и ферменты к митотической деятельности.
2. Пептид гена, родственного кальцитонину, стимулирует пролифе-рацию эндотелиальных клеток, а субстанция Р индуцирует выработку ФНО в мак-рофагах.
3. Простагландины группы Е потенцируют регенерацию путем усиления кровоснабжения.
4. Кейлоны и антикейлоны, продуцируемые различными клетками, дейст-вуя по принципу обратной связи, могут активировать и угнетать митотиче-ские процессы в очаге воспаления (Бала Ю.М., Лифшиц В.М., Сидельникова В.И., 1988).
5. Полиамины (путресцин, спермидин, спермин), обнаруживаемые во всех клетках млекопитающих, жизненно необходимы для роста и деления клеток.
Они обеспечивают стабилизацию плазматических мембран и суперспи-ральной структуры ДНК, защиту ДНК от действия нуклеаз, стимуляцию транскрипции, метилирование РНК и связывание ее с рибосомами, актива-цию ДНК-лигаз, эндонуклеаз, протеинкиназ и многие другие клеточные про-цессы. Усиленный синтез полиаминов, способствующих пролиферативным процессам, отмечается в очаге альтерации (Березов Т.Т., Федорончук Т.В., 1997).
6. Циклические нуклеотиды: цАМФ ингибирует, а цГМФ активирует про-цессы пролиферации.
Заживление раны.
Морфологически процесс заживления раны может протекать различно, в зависимости от анатомического субстрата поражения, степени инфицирован-ности, общего состояния организма, характера лечебных мероприятий (Ку-зин М.И., Костюченок Б.М. и соавт., 1990). Однако в любом случае течение раневого процесса отражает один из классических типов заживления:
1. Заживление первичным натяжением.
2. Заживление вторичным натяжением.
3. Заживление под струпом.
Заживление раны первичным натяжением. Такой тип заживления харак-теризуется сращением краев раны без видимой промежуточной ткани, путем соединительнотканной организации раневого канала. Заживление первичным натяжением является наиболее экономичным видом заживления. Для зажив-ления первичным натяжением необходимы следующие условия:
1. Небольшая зона повреждения.
2. Плотное соприкосновение краев раны.
3. Сохранение жизнеспособности краев раны.
4. Отсутствие очагов некроза и гематомы.
5. Асептичность раны.
Морфологическая картина заживления первичным натяжением проявля-ется умеренной гиперемией, отеком тканей в стенках раны, пролиферацией фибробластов и новообразованием капилляров путем эндотелизации каналов и щелей в сгущающемся фибрине (аутохтонный механизм) от одного края раны к противоположному. На 6-8-й день грануляционная ткань прочно со-единяет стенки раны, и в этот период прекращается эпителизация. В хирур-гической практике заживление первичным натяжением возможно в двух слу-чаях: при небольших размерах раны (края отстают не более 10 мм друг от друга), а также при хирургических вмешательствах, заканчивающихся нало-жением швов. Местные изменения в области раны выражены незначительно (отечность краев, гиперемия, инфильтрация, боль). К общим проявлениям относится повышение температуры тела, которая постепенно снижается к 3-м суткам после операции. Изменения морфологического состава крови вы-ражены незначительно или отсутствуют. Иногда отмечаются нейтрофильный лейкоцитоз и увеличение СОЭ до 20 мм/ч. На 5-6-е сутки эти показатели обычно нормализуются.
Заживление раны вторичным натяжением происходит при обширных по-вреждениях тканей, при наличии в ране нежизнеспособных тканей, гематомы и при развитии инфекции в ране. Любой из этих факторов ведет к заживле-нию вторичным натяжением. При различных вариантах течения заживления вторичным натяжением речь идет о заживлении гнойной раны, то есть о за-живлении через нагноение и гранулирование. На 5-6-е сутки после альтера-ции, после отторжения некротизированных клеток в ране появляются ост-ровки грануляций, которые, постепенно разрастаясь, заполняют всю полость раны. Изменения характера грануляций всегда объективно отражают ослож-нения заживления, которые могут наступить под влиянием местных и общих факторов. Реорганизация рубца проявляется активной эпителиизацией раны. Эпителий нарастает на поверхность грануляций в виде голубовато-белой каймы очень медленно. Помимо эпителизации заживлению способствует фе-номен раневой контракции — равномерного концентрического сокращения краев и стенок раны. Этот феномен объясняется появлением в грануляцион-ной ткани в период регенерации фибробластов, обладающих способностью к сокращению.
Заживление раны под струпом характерно для незначительных повреж-дений (ссадины, царапины, небольшие по площади ожоги 1-й и 2-й степени). Раневой процесс начинается свертыванием излившейся крови или только лимфы, которая подсыхает с образованием струпа. Под ним происходит бы-страя регенерация эпидермиса, и струп затем отторгается. Весь процесс длится 3-7 дней. Если заживление под струпом происходит без осложнений, то рана заживает первичным натяжением; если под струпом начинается на-гноение, то заживление идет по типу вторичного натяжения. В ряде случаев может развиться вялотекущее флегмонозное поражение жировой клетчатки, окружающей рану. В такой ситуации необходимы хирургическая обработка раны и удаление струпа (Кузин М.И., Костюченок Б.М. и соавт., 1990).
предыдущий раздел | содержание| следующий раздел
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 6 октября 2019;
проверки требует 1 правка.
Пролиферация (от лат. proles — отпрыск, потомство и fero — несу) — разрастание ткани организма путём размножения клеток делением.
История[править | править код]
Термин в медицине впервые ввел немецкий учёный Вирхов для обозначения новообразования клеток путём их размножения делением[1], дабы отличать этот механизм от других механизмов изменения объёма клеток, например отёка или апоптоза.
Регулирование пролиферации[править | править код]
Интенсивность пролиферации регулируется стимуляторами и ингибиторами, которые могут вырабатываться и вдали от реагирующих клеток (например, гормонами), и внутри них. Эффект стимулирования пролиферации используется в биоинженерии при создании модифицированных каркасов тканеинженерных конструкций[2].
Непрерывно пролиферация происходит в раннем эмбриогенезе и по мере дифференцировки периоды между делениями удлиняются.
Термин в философии[править | править код]
В философию данный термин внес Фейерабенд для обозначения процесса умножения (размножения) конкурирующих теорий. Философы употребляют термин при обозначении процесса привития или произрастания некоторой научной новации в науке.
Термин в ботанике[править | править код]
В ботанике пролиферация растения (пролификация) — это явление прорастания какого-либо органа из другого органа, завершившего свой рост. Например, формирование из апикальной меристемы цветка не гинецея, а побега с листьями.
Пролиферация в патологической анатомии животных[править | править код]
Это завершающая стадия воспаления с восстановлением повреждённой ткани или образованием рубца. Пролиферирующие фибробласты синтезируют основные вещества соединительной ткани — тропоколлаген и коллаген, которые превращаются в зрелые клетки-фиброциты. Формируются аргирофильные и коллагеновые волокна, грануляционная ткань с большим количеством вновь образованных капилляров и молодых клеток превращается в волокнистую соединительную ткань, которая замещает мёртвую ткань или служит барьером между здоровой и воспалённой частями органа[3].
Причиной пролиферативных явлений служит ряд активных веществ-стимуляторов роста и размножения, освобождающихся при распаде лейкоцитов и других клеточных элементов, и оптимальные сдвиги в осмотическом и онкотическом давлении. Действие этих веществ осуществляется рефлекторно, путём раздражения рецепторов поражённых тканей[4].
Примечания[править | править код]
- ↑ Большая медицинская энциклопедия (недоступная ссылка)
- ↑ Тенчурин Т.Х., Люндуп А.В., Демченко А.Г., и др. Модификация биодеградируемого волокнистого матрикса эпидермальным фактором роста при эмульсионном электроформовании для стимулирования пролиферации эпителиальных клеток // Гены и клетки. — 2017. — Т. 12, № 4. — С. 47-52. — ISSN 2313-1829. — doi:10.23868/201707029.
- ↑ А.В.Жаров, В.П.Шишков и др. Патологическая анатомия сельскохозяйственных животных. — М,: Колос, 1995. — 543 с.
- ↑ М.К.Долматов, А.А.Журавель, В.М.Коропов. Патологическая физиология сельскохозяйственных животных. — М., 1960. — 512 с.
Ссылки[править | править код]
Источник
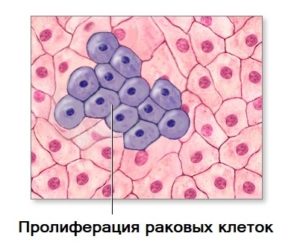 Пролиферация – это процесс размножения клеток, приумножающий объем тканей. Интенсивно протекает в период эмбрионального развития, когда клетки развивающегося эмбриона активно и непрерывно делятся. Процессом пролиферации управляют гормоны, способные как ускорить её, так и замедлить рост клеток.
Пролиферация – это процесс размножения клеток, приумножающий объем тканей. Интенсивно протекает в период эмбрионального развития, когда клетки развивающегося эмбриона активно и непрерывно делятся. Процессом пролиферации управляют гормоны, способные как ускорить её, так и замедлить рост клеток.
Пролиферация, являясь основным процессом, обеспечивающим нормальное развитие и рост тканевых структур, способствует их постоянному обновлению и нормальной работе организма.
Пациенты, увидев в заключении врача после обследования слово «пролиферация», задаются вопросом что это такое, начинают волноваться насколько это опасно, но не стоит паниковать – пролиферация не является заболеванием.
Клеточным структурам многих видов тканей необходимо регулярное обновление. Этот физиологический процесс осуществляется путем деления клеток. Процесс обновления клеток явно выражен в кожном покрове, слизистых оболочках желудочно-кишечного тракта, системы дыхания и матки. Это означает, что пролиферация в них является необходимым и нормальным процессом.
Клеточная пролиферация с медицинской точки зрения
 Изучив процесс клеточной пролиферации, врачи выяснили, что она контролирует процесс нормального функционирования защитных сил организма – иммунитета. Пролиферация способствует уничтожению тканевых дефектов и восстановлению прежнего функционирования органов, работа которых была нарушена. Но нельзя назвать пролиферацию полностью безвредным процессом. Она может принимать участие и в патологических процессах, например, при выработке большого количества соматотропного гормона (гормона роста) наблюдается увеличение конечностей и некоторых органов.
Изучив процесс клеточной пролиферации, врачи выяснили, что она контролирует процесс нормального функционирования защитных сил организма – иммунитета. Пролиферация способствует уничтожению тканевых дефектов и восстановлению прежнего функционирования органов, работа которых была нарушена. Но нельзя назвать пролиферацию полностью безвредным процессом. Она может принимать участие и в патологических процессах, например, при выработке большого количества соматотропного гормона (гормона роста) наблюдается увеличение конечностей и некоторых органов.
Нарушение процесса пролиферации и дифференцировки клеток может сопровождаться атипией (внешнее и функциональное изменение клеток) и дать толчок образованию злокачественных опухолей. Клетки начинают активно размножаться, что называется гиперпролиферация. Так происходит потому, что пролиферация уже не дифференцирующихся клеток приводит к началу опухолевого процесса. Но не следует забывать о том, что в различных органах тканевая пролиферация протекает неодинаково.
Ведущие клиники в Израиле
В зависимости от индекса пролиферативной активности и способности делиться клетки организма в медицине подразделяются на 3 группы:
- Лабильные;
- Стабильные;
- Статические.
Лабильным клеткам присущи выраженные пролиферативные процессы, вследствие чего они могут регенерировать быстро и восстанавливать свою деятельность.
В процессе регенерации наблюдаются такие процессы как:
- Рост соединительной ткани;
- Формирование новых сосудов;
- Устранение тканевых дефектов.
В эту группу можно включить клетки крови, эпителиальной ткани и эпидермиса, слизистого покрова желудочно-кишечного тракта. Наиболее быстро пролиферация протекает в слизистой желудка.
Стабильным клеткам свойственны умеренные пролиферативные процессы из-за чего способность их к быстрому размножению и восстановлению несколько хуже. Пролиферирующие клетки здесь образуются исключительно в результате серьезных повреждений тканей или органов. Сюда можно отнести печень, поджелудочную железу, поперечно-полосатую мышечную ткань, слюнные железы и др.
К статическим клеткам можно отнести кардиомиоциты и нервные клетки. Они практически не поддаются пролиферации, не способны восстанавливаться и размножаться. Однако, если на кардиомиоциты долгое время действует какое-либо напряжение, они способны восстановиться за счет пролиферирующих внутриклеточных структур внутри здоровых клеток. Это, в конечном счете, может привести к гипертрофии миокарда.
Виды пролиферации
Медицине на сегодняшний день известны следующие виды пролиферации клеток:
- Физиологическая пролиферация – восстанавливает тканевые и клеточные структуры естественным путем. Сюда можно отнести пролиферацию плоского эпителия ЖКТ и клеток крови;
- Репаративная — способствует регенерации тканей и клеточных структур при воспалительных процессах после каких-либо повреждений;
- Патологическая пролиферация клеток – процесс развития атипичных тканей, отличающихся структурой от здоровых. В пример можно привести рубцы в месте ожогов, разрастание соединительных тканей в месте разрыва стенки миокарда, хрящи в месте перелома. Но самым сложным проявлением патологической пролиферации является возникновение раковых опухолей.
Изучение процессов пролиферации имеет немаловажное значение для понимания процесса гомеостаза (поддержания постоянства внутренней среды организма).
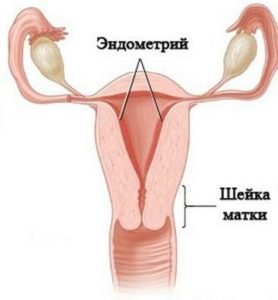
Пролиферация эндометрия и шейки матки
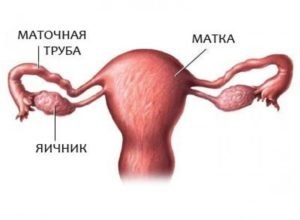 Пролиферация в гинекологии – явление нередкое. Деление клеток женских половых органов итак происходит довольно быстро, а при патологиях этот процесс протекает еще активнее. Пролиферация клеток призматического эпителия в половых органах выявляется после гистологического анализа слизистой оболочки матки, шейки матки или ее фрагмента, который забирается путем конизации. По итогам анализа врач-гинеколог делает вывод о наличии или отсутствии патологического процесса.
Пролиферация в гинекологии – явление нередкое. Деление клеток женских половых органов итак происходит довольно быстро, а при патологиях этот процесс протекает еще активнее. Пролиферация клеток призматического эпителия в половых органах выявляется после гистологического анализа слизистой оболочки матки, шейки матки или ее фрагмента, который забирается путем конизации. По итогам анализа врач-гинеколог делает вывод о наличии или отсутствии патологического процесса.
Рассмотрим подробнее пролиферацию в матке. В разных частях матка имеет неодинаковую структуру и выстилку. Шейку ее выстилает многослойный плоский без атипии эпителий, зону цервикального канала – цилиндрический эпителий, а слизистую эндометрия выстилает железистая ткань.
В течение одного менструального цикла на матку воздействуют гормональные всплески, готовящие ее к возможной беременности, поэтому клетки ее начинают пролиферировать и подготавливать эндометрий для более удобной имплантации оплодотворенной яйцеклетки. Именно поэтому процесс пролиферации не просто нормальный, но еще и необходимый.
У беременной женщины в результате гормональных изменений активная пролиферация железистого эпителия маточной шейки считается нормальным явлением.
Ускоренный пролиферативный процесс может свидетельствовать о следующем:
- О наличии воспалительного процесса – цервицита;
- О повреждениях различного рода (выскабливание при абортах, послеродовые разрывы, удаление фрагмента шейки матки);
- О возможных опухолевых процессах (дисплазия, полипы, рак).
Иными словами, в шейке матки наблюдается воспалительная, гиперпластическая и посттравматическая пролиферация.
Бактериальные, грибковые и вирусные цервициты приводят к повреждениям покровного эпителия, который вследствие этого начинает усиленно пролиферировать для восстановления своей целостности.
Похожие явления наблюдаются при эрозии, повреждении шейки матки при родовых потугах, абортах и прочих манипуляциях. Такая пролиферация, способствующая регенерации многослойной плоской эпителиальной ткани, считается физиологической.
Пролиферация в перечисленных выше ситуациях не приносит вреда, но все же требует лечения под наблюдением врача. При полном восстановлении слизистой оболочки волноваться не о чем.
Пролификация с атипией имеет несколько другой характер. Базальноклеточная гиперплазия может способствовать развитию псевдоэрозий шейки матки, которые при несвоевременном лечении могут преобразоваться в раковую опухоль.
Псевдоэрозия представляет собой явление, когда снаружи шейки матки появляются участки железистого эпителия, который обычно выстилает стенки в цервикальном канале. Это происходит из-за гормонального сбоя, который в свою очередь вызывается вирусными заболеваниями. При псевдоэрозиях может пролиферировать, как плоский эпителий, так и участки цилиндрического, из которого и формируются эрозии.
Опасным явлением выступает пролиферация с дисплазией многоклеточного плоского эпителия шейки матки, так как дисплазия – это предраковый процесс.
Поговорим о пролиферации эндометрия.
 Эндометрий представляет собой внутренний слой матки, постоянно обновляющийся и имеющий сложное строение. В период менструации он отторгается из-за не наступившей беременности и образуется вновь до следующего цикла. Этот процесс является постоянным и не обходится без пролиферации. Более активно клетки эндометрия пролиферируют в первую половину менструального цикла, когда слизистая оболочка матки находится под действием гормонов эстрогенов. В случае, когда пролиферация не прекратилась вовремя, возникает гиперплазия эндометрия. Это может повлечь за собой образование кист, полипов, что грозит перерождением их в онкологию.
Эндометрий представляет собой внутренний слой матки, постоянно обновляющийся и имеющий сложное строение. В период менструации он отторгается из-за не наступившей беременности и образуется вновь до следующего цикла. Этот процесс является постоянным и не обходится без пролиферации. Более активно клетки эндометрия пролиферируют в первую половину менструального цикла, когда слизистая оболочка матки находится под действием гормонов эстрогенов. В случае, когда пролиферация не прекратилась вовремя, возникает гиперплазия эндометрия. Это может повлечь за собой образование кист, полипов, что грозит перерождением их в онкологию.
Получается, процесс пролиферации в матке не всегда является патологией. В некоторых случаях этот процесс жизненно необходим.
Пролиферация клеток в гастроэнтерологии
Обновление клеток железистого эпителия желудка происходит регулярно, так как она нуждается в постоянной пролиферации. Любое повреждение слизистой ускоряет процесс деления клеток. Причинами активной пролиферации обычно выступают язвенная болезнь, гастрит, различные полипы, а также опухоль.
При острой форме гастрита на фоне воспаления, выраженного в виде отечности слизистого покрова и кровоизлияний, выявляются также участки покровно-ямочного эпителия, который пролиферируя, способствует регенерации поврежденной слизистой оболочки.
Хронический гастрит, встречающийся сегодня у людей всех возрастных групп, также протекает с усиленным процессом пролиферации эпителия. Этот процесс особенно проявляется при гиперплазиях, когда утолщается слизистая и возможно возникновение различного рода полипов.
При обострении язвенной болезни наблюдается повреждение стенок органа. Для устранения этого дефекта по краям язвы начинается активная пролиферация слизистого эпителия. Такая пролиферация особенно характерна для гиперпластических полипов, обнаруживаемых по краям язвы.
Наиболее опасной считается предраковая пролиферация желудочной стенки, когда начинает умножаться количество темных вытянутых клеток в зоне шеек желез желудка.
В самом начале процесс несет регенеративный характер, но из-за нарушенной дифференцировки клеток полного восстановления слизистой не наблюдается. Железы в результате покрываются несвойственными ими темными вытянутыми клетками, которые в норме находятся лишь в шейках этих желез. В дальнейшем это приводит к развитию злокачественного образования – карциномы.
Пролиферация молочной железы
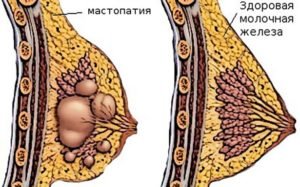 Молочные железы часто подвержены различным изменениям. Они регулярно испытывают на себе воздействие половых гормонов, которое проявляется в изменениях груди во время менструации, в период беременности и грудного вскармливания. По этой причине орган подвержен различным патологиям. Согласно статистическим данным около 60% женщин в возрасте 25-35 лет подвержены развитию мастопатии.
Молочные железы часто подвержены различным изменениям. Они регулярно испытывают на себе воздействие половых гормонов, которое проявляется в изменениях груди во время менструации, в период беременности и грудного вскармливания. По этой причине орган подвержен различным патологиям. Согласно статистическим данным около 60% женщин в возрасте 25-35 лет подвержены развитию мастопатии.
Несмотря на то, что мастопатия является доброкачественным процессом, наличие ее повышает риск развития рака груди. Пролиферативное действие здесь еще более опасно. Оно повышает риск развития онкологии в 25 раз. Именно поэтому пролиферуриющая мастопатия называется предраковой.
Не тратьте время на бесполезный поиск неточной цены на лечение рака
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
Выделяют 3 степени мастопатии:
- При первой степени не наблюдается пролиферации;
- При второй имеются признаки пролиферации;
- При третьей степени наблюдается выраженная пролиферация атипичных клеток эпителия.
Получается, процесс пролиферации является не только признаком развития мастопатии, но и показателем возможного развития онкологии. Поэтому при наличии каких-либо изменений в груди делается цитограмма для изучения структуры ткани груди.
Пролиферация при воспалениях
Любой воспалительный процесс завершается пролиферацией. Очаговая воспаленная часть ограничивается от нормальных тканей именно за счет пролиферации. Однако, этот процесс может наблюдаться на начальной стадии воспаления фолликулярного эпителия. В этом случае причины пролиферации могут быть разнообразными.
В процессе пролиферации может наблюдаться активное деление различных клеток, а именно:
- Клеток мезенхимы;
- Эндотелиальных клеток;
- В — и Т-лимфоцитов;
- Клеток адвентиция;
- Тучных клеток;
- Макроцитарных клеток.
Рассмотрим пролиферацию в фибробластах. При ней наблюдается активная выработка белков. В дальнейшем фибробласты преобразуются в зрелые клетки, именуемые фиброцитами. На конечном этапе пролиферация приводит к отделению очага воспаления от нормальных тканей с помощью коллагена. Смотря на наличие такой структуры, можно установить диагноз пролиферация.
Что делать при выявлении пролиферации?

Где бы ни был выявлен процесс пролиферации, первое, что сделает квалифицированный специалист – это определит причину, только потом подберет необходимую терапию. Не существует однозначного метода лечения пролиферации, так как она не является самостоятельной патологией, а лишь служит спутником других болезней.
Для лечения пролиферации при воспалительных процессах назначается противовоспалительная терапия, дополняющаяся противовирусными и антибактериальными препаратами, оказывающими антипролиферативное действие.
Предраковый пролиферат с атипией на фоне фовеолярной дисплазии требует более серьезных мер лечения вплоть до удаления пораженной части органа или ткани. Пролиферация, протекающая на фоне карциномы, требует лечения по правилам онкологической терапии и не исключает удаления пораженного органа.
Пролиферация, которая свидетельствует о патологии, служит сигналом, призывающим к немедленному лечению. В связи с этим пациенты с диагностированной у них пролиферацией, находятся под надзором врача. Завершив лечение основного заболевания, следует провести дополнительное исследование (биопсию или цитологический анализ), которое позволит оценить насколько эффективно прошло лечение и определить есть ли риск образования в будущем злокачественной опухоли.
Источник

