Перекисное окисление липидов при воспалении

РАЗДЕЛ 8. ОБМЕН ЛИПИДОВ
VII. Перекисное окисление липидов, роль в патогенезе повреждений клетки
Кислород, необходимый организму для функционирования ЦПЭ и многих других реакций, является одновременно и токсическим веществом, если из него образуются так называемые активные формы.
К активным формам кислорода относят:
ОН• — гидроксильный радикал;
О2• — супероксидный анион;
Н2O2 — пероксид водорода.
Активные формы кислорода образуются во многих клетках в результате последовательного одноэлектронного присоединения 4 электронов к 1 молекуле кислорода. Конечный продукт этих реакций — вода, но по ходу реакций образуются химически активные формы кислорода. Наиболее активен гидроксильный радикал, взаимодействующий с большинством органических молекул. Он отнимает от них электрон и инициирует таким образом цепные реакции окисления. Эти свободнорадикальные реакции окисления могут выполнять полезные функции, например, когда клетки белой крови с участием активных форм кислорода разрушают фагоцитированные клетки бактерий. Но в остальных клетках свободнорадикальное окисление приводит к разрушению органических молекул, в первую очередь липидов, и, соответственно, мембранных структур клеток, что часто заканчивается их гибелью. Поэтому в организме функционирует эффективная система ингибирования перекисного окисления липидов (ПОЛ).
А. Источники активных форм кислорода
ЦПЭ как источник активных форм кислорода
Утечка электронов из ЦПЭ и непосредственное их взаимодействие с кислородом — основной путь образования активных форм кислорода в большинстве клеток.
Кофермент Q в ЦПЭ принимает от доноров последовательно по одному электрону, превращаясь в форму семихинона (рис. 8-55) — КоQН• (см. раздел 6).
Этот радикал может непосредственно взаимодействовать с кислородом, образуя супероксидный анион О2•, который, в свою очередь, может превращаться в другие активные формы кислорода:
![]()
Рис. 8-55. Реакции последовательного восстановления убихинона в дыхательной цепи.

Реакции, катализируемые оксидазами и оксигеназами
Многие оксидазы — ферменты, непосредственно восстанавливающие кислород, образуют пероксид водорода — Н2O2. Оксидазы образуют пероксид водорода по схеме:
O2 + SН2 —> S + Н2O2, где SН2 — окисляемый субстрат.
Примеры таких оксидаз — оксидазы аминокислот, супероксид дисмутаза, оксидазы, локализованные в пероксисомах. Оксидазы пероксисом окисляют, в частности, жирные кислоты с очень длинной углеродной цепью (более 20 углеродных атомов) до более коротких, которые далее подвергаются β-окислению в митохондриях.
Монооксигеназы, например, цитохром Р450, включающий один атом кислорода в окисляемую молекулу, и диоксигеназы, включающие оба атома кислорода, также служат источниками активных форм кислорода.
Пероксид водорода химически не очень активен, но способствует образованию наиболее токсичной формы кислорода — гидроксильного радикала (ОН•) по следующей реакции:
Fе2+ + Н2O2 —>Fе3+ + ОН- + ОН•.
Наличие в клетках Fе2+ или ионов других переходных металлов увеличивает скорость образования гидроксильных радикалов и других активных форм кислорода. Например, в эритроцитах окисление иона железа гемоглобина способствует образованию супероксидного аниона.
Б. Перекисное окисление липидов
Реакции перекисного окисления липидов (ПОЛ) являются свободнорадикальными и постоянно происходят в организме. Свободнорадикальное окисление нарушает структуру многих молекул. В белках окисляются некоторые аминокислоты. В результате разрушается структура белков, между ними образуются ковалентные «сшивки», всё это активирует протеолитические ферменты в клетке, гидролизующие повреждённые белки. Активные формы кислорода легко нарушают и структуру ДНК. Неспецифическое связывание Fе2+молекулой ДНК облегчает образование гидроксильных радикалов, которые разрушают структуру азотистых оснований. Но наиболее подвержены действию активных форм кислорода жирные кислоты, содержащие двойные связи, расположенные через СН2-группу. Именно от этой СН2-группы свободный радикал (инициатор окисления) легко отнимает электрон, превращая липид, содержащий эту кислоту, в свободный радикал.
ПОЛ — цепные реакции, обеспечивающие расширенное воспроизводство свободных радикалов, частиц, имеющих неспаренный электрон, которые инициируют дальнейшее распространение перекисного окисления.
Стадии перекисного окисления липидов
1) Инициация: образование свободного радикала (L•)

Инициирует реакцию чаще всего гидроксильный радикал, отнимающий водород от СН2-групп полиеновой кислоты, что приводит к образованию липидного радикала.
2) Развитие цепи:
![]()
Развитие цепи происходит при присоединении O2, в результате чего образуется липопероксирадикал LOO• или пероксид липида LOOH.
ПОЛ представляет собой свободнорадикальные цепные реакции, т.е. каждый образовавшийся радикал инициирует образование нескольких других.
3) Разрушение структуры липидов

Конечные продукты перекисного окисления полиеновых кислот — малоновый диальдегид и гидропероксид кислоты.
4) Обрыв цепи — взаимодействие радикалов между собой:

Развитие цепи может останавливаться при взаимодействии свободных радикалов между собой или при взаимодействии с различными антиоксидантами, например, витамином Е, который отдаёт электроны, превращаясь при этом в стабильную окисленную форму.
В. Повреждение клеток в результате перекисного окисления липидов
Активные формы кислорода повреждают структуру ДНК, белков и различные мембранные структуры клеток. В результате появления в гидрофобном слое мембран гидрофильных зон за счёт образования гидропероксидов жирных кислот в клетки могут проникать вода, ионы натрия, кальция, что приводит к набуханию клеток, органелл и их разрушению. Активация перекисного окисления характерна для многих заболеваний: дистрофии мышц (болезнь Дюшенна), болезни Паркинсона, при которых ПОЛ разрушает нервные клетки в стволовой части мозга, при атеросклерозе, развитии опухолей. Перекисное окисление активируется также в тканях, подвергшихся сначала ишемии, а затем реоксигенации, что происходит, например, при спазме коронарных артерий и последующем их расширении.
Такая же ситуация возникает при образовании тромба в сосуде, питающем миокард. Формирование тромба приводит к окклюзии просвета сосуда и развитию ишемии в соответствующем участке миокарда (гипоксия ткани). Если принять быстрые лечебные меры по разрушению тромба, то в ткани восстанавливается снабжение кислородом (реоксигенация). Показано, что в момент реоксигенации резко возрастает образование активных форм кислорода, которые могут повреждать клетку. Таким образом, даже несмотря на быстрое восстановление кровообращения, в соответствующем участке миокарда происходит повреждение клеток за счёт активации перекисного окисления.
Изменение структуры тканей в результате ПОЛ можно наблюдать на коже: с возрастом увеличивается количество пигментных пятен на коже, особенно на дорсальной поверхности ладоней. Этот пигмент называют липофусцин, представляющий собой смесь липидов и белков, связанных между собой поперечными ковалентными связями и денатурированными в результате взаимодействия с химически активными группами продуктов ПОЛ. Этот пигмент фагоцитируется, но не гидролизуется ферментами лизосом, и поэтому накапливается в клетках, нарушая их функции.
ПОЛ происходит не только в живых организмах, но и в продуктах питания, особенно при неправильном приготовлении и хранении пищи. Прогоркание жиров, образование более тёмного слоя на поверхности сливочного масла, появление специфического запаха у молочных продуктов — всё это признаки ПОЛ. В продукты питания, содержащие ненасыщенные липиды, обычно добавляют антиоксиданты — вещества, ингибирующие ПОЛ и сохраняющие структуру компонентов пищи.
Г. Системы защиты клеток от активных форм кислорода
Ферменты антиоксидантного действия
К ферментам, защищающим клетки от действия активных форм кислорода, относят супероксиддисмутазу, каталазу и глутатионпероксидазу. Наиболее активны эти ферменты в печени, надпочечниках и почках, где содержание митохондрий, цитохрома Р450 и пероксисом особенно велико. Супероксиддисмутаза (СОД) превращает супероксидные анионы в пероксид водорода:
2 О2• + 2 Н+ —> Н2О2 + О2.
Изоферменты СОД находятся и в цитозоле и в митохондриях и являются как бы первой линией защиты, потому что супероксидный анион образуется обычно первым из активных форм кислорода при утечке электронов из дыхательной цепи.
СОД — ицдуцируемый фермент, т. е. синтез его увеличивается, если в клетках активируется перекисное окисление.
Пероксид водорода, который может инициировать образование самой активной формы ОН•, разрушается ферментом каталазой:
2 Н2О2 —> 2 Н2О + О2.
Каталаза находится в основном в пероксисомах, где образуется наибольшее количество пероксида водорода, а также в лейкоцитах, где она защищает клетки от последствий «респираторного взрыва» (см. раздел 6).
Глутатионпероксидаза — важнейший фермент, обеспечивающий инактивацию активных форм кислорода, так как он разрушает и пероксид водорода и гидропероксиды липидов. Он катализирует восстановление пероксидов с помощью трипептида глутатиона (y-глутамилцистеинилглицин). Сульфгидрильная группа глутатиона (GSН) служит донором электронов и, окисляясь, образует дисульфидную форму глутатиона, в которой 2 молекулы глутатиона связаны через дисульфидную группу.
Н2O2 + 2 GSH —> 2 Н2O + G-S-S-G.
Окисленный глутатион восстанавливается глутатионредуктазой:
GS-SG + NADPH + Н+ —> 2 GSH + NADP+.
Глутатионпероксидаза, которая восстанавливает гидропероксиды липидов в составе мембран, в качестве кофермента использует селен (необходимый микроэлемент пищи). При его недостатке активность антиоксидантной защиты снижается.
Витамины, обладающие антиоксидантным действием
Витамин Е (α-токоферол) — наиболее распространённый антиоксидант в природе — является липофильной молекулой, способной инактивировать свободные радикалы непосредственно в гидрофобном слое мембран и таким образом предотвращать развитие цепи перекисного окисления. Различают 8 типов токоферолов, но α-токоферол наиболее активен.
Витамин Е отдаёт атом водорода свободному радикалу пероксида липида (ROO•), восстанавливая его до гидропероксида (ROOH) и таким образом останавливает развитие ПОЛ (рис. 8-56).
Рис. 8-56. Механизм антиоксидантного действия витамина Е. Витамин Е (α-токофероп) ингибирует свободнорадикальное окисление путём отдачи электрона, что приводит к инактивации радикала липида, а витамин Е превращается в стабильный, полностью окисленный токоферолхинон.

Свободный радикал витамина Е, образовавшийся в результате реакции, стабилен и не способен участвовать в развитии цепи. Наоборот, радикал витамина Е непосредственно взаимодействует с радикалами липидных перекисей, восстанавливая их, а сам превращается в стабильную окисленную форму — токоферолхинон.
Витамин С (аскорбиновая кислота) также является антиоксидантом и участвует с помощью двух различных механизмов в ингибировании ПОЛ. Во-первых, витамин С восстанавливает окисленную форму витамина Е и таким образом поддерживает необходимую концентрацию этого антиоксиданта непосредственно в мембранах клеток. Во-вторых, витамин С, будучи водорастворимым витамином и сильным восстановителем, взаимодействует с водорастворимыми активными формами кислорода — O2•, Н2O2, ОН• и инактивирует их.
β-Каротин, предшественник витамина А, также обладает антиоксидантным действием и ингибирует ПОЛ. Показано, что растительная диета, обогащённая витаминами Е, С, каротиноидами, существенно уменьшает риск развития атеросклероза и заболеваний ССС, подавляет развитие катаракты — помутнения хрусталика глаза, обладает антиканцерогенным действием. Имеется много доказательств в пользу того, что положительное действие этих компонентов пищи связано с ингибированием ПОЛ и других молекул и, следовательно, с поддержанием нормальной структуры компонентов клеток.
Источник
Перекисное окисление липидов (ПОЛ)
Реакции ПОЛ являются свободнорадикальными и постоянно протекают в организме, также как и реакции образования АФК.
В норме они поддерживаются на определенном уровне и выполняют ряд функций:
1. индуцируют апоптоз (запрограммированную гибель клеток);
2. регулируют структуру клеточных мембран и тем самым обеспечивают функционирование ионных каналов, рецепторов, ферментных систем;
3. обеспечивают освобождение из мембраны арахидоновой кислоты, из которой синтезируются биорегуляторы (простагландины, тромбоксаны, лейкотриены);
4. ПОЛ может выступать в качестве вторичного мессенджера, участвуя в трансформации сигналов из внешней и внутренней среды организма, обеспечивая их внутриклеточную передачу;
5. АФК участвуют в клеточном иммунитете и фагоцитозе.
Механизм ПОЛ:
1. Инициация. Инициирует реакцию чаще всего гидроксильный радикал, отнимающий водород от СН2- групп ненасыщенной жирной кислоты L, что приводит к образованию липидного радикала L•:
L + •OН ? L•
2. Развитие цепи. Развитие цепи происходит при присоединении кислорода, в результате чего образуется пероксидный радикал LOO• или пероксид липида LOOH (гидроперекиси липидов)
L• + O2 ? LOO•
LOО• + LH ? LOOH + LR?•
3. Обрыв цепи. Развитие цепи может останавливаться при взаимодействии свободных радикалов между собой или при взаимодействии с различными антиоксидантами (витамином Е), которые являются донорами электронов:
LOO•? + L• ? LOOH + LH
L?•+ Витамин Е ? LH + Витамин Е•?
ВитаминТ Е• + L• ? LH + Витамин Е окисл
В результате ПОЛ происходит преобразование обычных липидов в первичные продукты ПОЛ (гидроперекиси липидов). Это приводит к появлению в мембранах участков («дыр»), через которые наружу выходит содержимое как самих клеток, так и их органелл.
Первичные продукты ПОЛ разрушаются с образованием вторичных продуктов ПОЛ: альдегидов, кетонов, малонового диальдегида, диеновых коньюгатов. Накоплением в крови малонового диальдегида (МДА) объясняется синдром интоксикации, сопровождающий многие заболевания внутренних органов. Реагируя с SH- и СН3-группами белков, МДА подавляет активность цитохром-оксидаз (угнетая тем самым тканевое дыхание) и гидроксилаз. МДА обуславливает также ускоренное развитие атеросклероза.
При взаимодействии МДА с аминогруппами фосфолипидов образуются конечные продукты ПОЛ – Шиффовы основания. Примером этих соединений является пигмент липофусцин, появляющийся на оболочке глаза, на коже с возрастом. Липофусцин представляет собой смесь липидов и белков, связанных между собой поперечными ковалентными связями и денатурированными в результате взаимодействия с химически активными группами продуктов ПОЛ. Этот пигмент фагоцитируется, но не гидролизуется ферментами лизосом, накапливается в клетках, нарушая их функцию.
Негативные последствия активации ПОЛ:
1. Повреждение липидного бислоя мембран, в результате чего в клетки проникает вода, ионы натрия, кальция, что приводит к набуханию клеток, органелл и их разрушению.
2. Преждевременное старение клеток и организма в целом.
3. Взаимодействие высокореактивных продуктов ПОЛ с аминогруппами белков с образованием Шиффовых оснований.
4. Изменение текучести (вязкости) мембран, в результате чего нарушается транспортная функция мембран (функционирование ионных каналов).
5. Нарушение активности мембраносвязанных ферментов, рецепторов.
Активация ПОЛ характерна для многих заболеваний и патологических состояний:
1. атеросклероз и другие сердечнососудистого заболевания;
2. поражения ЦНС (болезнь Паркинсона, Альцгеймера);
3. воспалительные процессы любого генеза;
4. дистрофия мышц (болезнь Дюшенна);
5. онкологические заболевания;
6. радиационные поражения;
7. бронхолегочные патологии.
Данный текст является ознакомительным фрагментом.
Похожие главы из других книг:
Глава 10. Энергетический обмен. Биологическое окисление
Живые организмы с точки зрения термодинамики – открытые системы. Между системой и окружающей средой возможен обмен энергии, который происходит в соответствии с законами термодинамики. Каждое органическое
Глава 19. Липиды тканей, переваривание и транспорт липидов
Липиды – неоднородная в химическом отношении группа веществ биологического происхождения, общим свойством которых является гидрофобность и способность растворяться в неполярных органических растворителях.
Глава 21. Обмен сложных липидов
К сложным липидам относят такие соединения, которые, помимо липидного, содержат и нелипидный компонент (белок, углевод или фосфат). Соответственно существуют протеолипиды, гликолипиды и фосфолипиды. В отличие от простых липидов,
2.5. Биологическое окисление
Анализируя отдельные этапы клеточного метаболизма, всегда необходимо помнить, что он представляет собой единый, интегральный, взаимосвязанный механизм (Бохински Р., 1987). Процессы анаболизма и катаболизма происходят в клетке одновременно и
Источник
Перекисное окисление липидов (ПОЛ) представляет собой жизненно необходимое звено метаболического обмена. Основная функция его заключается в обновлении липидов клеточных мембран.
У здорового человека процессы перекисного окисления липидов контролируются так называемой антиокислительной системой, которая регулирует скорость и активность фосфорилирования путем связывания провоцирующих факторов или нейтрализации достаточного количества перекисей, чтобы не допустить переизбыток конечных продуктов обмена. Усиление процесса окисления может стать отправной точкой в патофизиологических процессах значительного количества заболеваний. Этот процесс включает в себя стадии ферментативного и неферментативного аутоокисления.
Виды
Для модификации фосфолипидного бислоя клеточных мембран проходит ферментативное окисление. Кроме того, он участвует в образовании биологически активных веществ, детоксикации организма, метаболических реакциях. Неферментативное же окисление проявляет себя как разрушающий фактор в жизни клетки. Из-за образования большого количества свободных радикалов и накопления перекисей активность антиоксидантной системы снижается и, как следствие, наблюдается гибель клеток организма.
Цикл ПОЛ
Для начала перекисного окисления липидов необходимо наличие свободных радикалов кислорода, имеющих на крайнем энергетическом уровне один неспаренный электрон. После восстановления молекулы образуется супероксид кислорода, который реагирует с атомами водорода, превращаясь в перекись водорода. Для регулирования количества супероксидов внутри клетки существуют супероксиддисмутаза, образующая перекись водорода, а каталаза, пероксидаза нейтрализуют ее до воды. Если живой организм подвергся действию ионизирующего излучения, количество свободных гидроксильных радикалов резко увеличится. Кроме гидроксида кислорода и другие его активные формы могут выступать инициаторами запуска процесса перекисного окисления липидов.
Продукты перекисного окисления липидов либо утилизируются организмом, либо используются для синтеза простагландинов (веществ, участвующих в реакциях воспаления), тромбоксанов (входят в каскад тромбообразующих реакций), гормонов надпочечников.
Система контроля
В зависимости от базовой структуры мембраны клетки скорость, активность и количество получившихся продуктов окисления могут варьироваться. Так, например, активность перекисного окисления липидов выше там, где в составе клеточной стенки преобладают ненасыщенные жирные кислоты, и медленнее, если основой КС является холестерин. Кроме того, фактором, регулирующим количество и скорость образования свободных кислородных радикалов, а также утилизацию перекисей, являются метаболические ферменты. Еще в реакции перекисного окисления липидов принимают участие вещества, влияющие на липидный состав мембраны клетки и его произвольное изменение в соответствии с потребностями организма. К ним относятся витамин Е и К, тироксин (гормон щитовидной железы), гидрокортизон, кортизон и альдостерон (по принципу обратной связи). Дестабилизируют клеточную стенку ионы металлов, витамины С и D.
Нарушение процесса
Метаболические продукты перекисного окисления липидов могут накапливаться в тканях и жидкостях организма, если антиоксидантная система не успевает утилизировать их с необходимой скоростью. Вследствие этого нарушается транспорт ионов через мембрану клетки, что опосредованно может влиять на ионный состав жидкой части крови, скорость поляризации и деполяризации мембран мышечных клеток (нарушать проводимость нервных импульсов, их сократимость, увеличивать рефрактерный период), способствовать выходу жидкости во внеклеточное пространство (отеки, сгущение крови, нарушение электролитного баланса). Кроме того, основные продукты перекисного окисления липидов, после ряда биохимических реакций, превращаются в альдегиды, кетоновые тела, кислоты и пр. Эти вещества оказывают токсическое влияние на организм, проявляющееся в снижении скорости синтеза ДНК, повышении проницаемости капилляров, повышении онкотического давления и, как следствие, сладж-синдроме.
Проявления в клинике
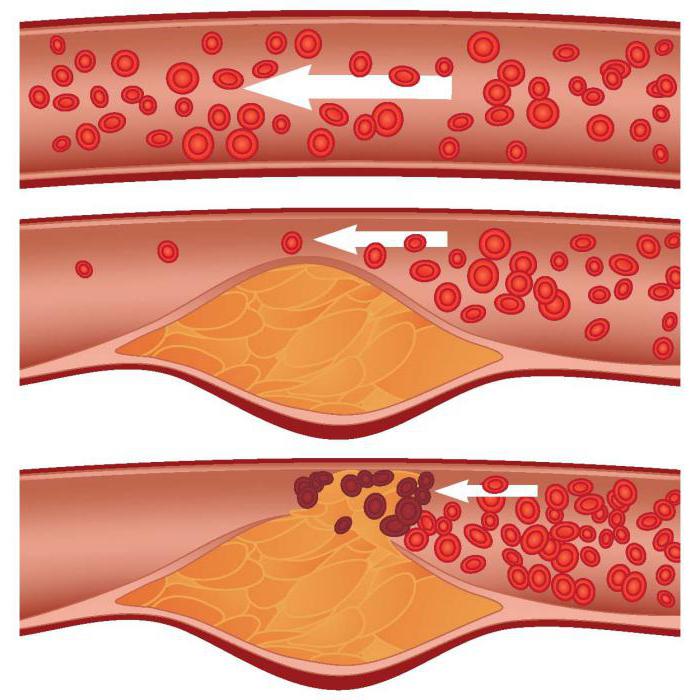
Так как увеличение количества свободных радикалов кислорода оказывает повреждающее влияние на клеточную стенку, а продукты обмена нарушают процесс метаболизма и синтеза нуклеиновых кислот, а также отравляют организм, они являются патофизиологическим фактором развития ряда клинических состояний. Роль перекисного окисления липидов является немаловажной при заболеваний печени, суставов, паразитарных инфекционных заболеваний, нарушениях гемодинамики, онкологических заболеваниях, травмах и ожогах. ПОЛ выступает одним из факторов развития атеросклероза. Свободные радикалы, окисляя холестерин и его низкомолекулярные фракции, образуют продукты, повреждающие сосудистую стенку. При этом запускается каскад типичных патологических реакций, направленных на устранение повреждения. Это провоцирует тромбообразование, накопление сгустков крови в просвете мелких сосудов или прикрепление к их стенкам. В результате движение крови на этом участке замедляется, так как просвет сосуда стал уже. Это способствует дальнейшему накоплению тромбов. Наиболее подвержены подобным изменениям коронарные артерии, аорта, проявляющиеся в клинике как симптомы ишемической болезни сердца.
Превентивные меры

Практикующим специалистам необходимо помнить, что проведение диагностических и лечебных процедур может активировать механизм перекисного окисления липидов. Об этом следует предупредить пациента. К провоцирующим факторам относятся лучевая терапия (при онкологии), ультрафиолетовое облучение (при рахите, воспалительных заболеваниях пазух носа, антибактериальной обработке помещений), магнитные поля (МРТ, КТ, физиотерапия), сеансы в барокамере (при полиомиелите, горной болезни).
Профилактика и терапия

Персоналу, работающему в рентгенкабинетах, санитаркам и медсёстрам, специалистам по физиотерапии, альпинистам, людям с избыточным весом нужно употреблять в пищу продукты, содержащие естественные антиоксиданты: рыбу, подсолнечное или оливковое масло, зелень, яйца, зеленый чай.
Помимо изменения диеты, можно использовать лекарственные средства, которые связывают некоторые группы свободных радикалов или соединяются с металлами переменной валентности. Таким образом они замещают свободные молекулы активного кислорода, не давая им связываться с усилителями ПОЛ.
Диагностика
На нынешнем этапе развития лабораторных исследований мы имеем возможность обнаружить перекиси в составе биологических жидкостей организма человека. Для этого нужно провести флуоресцентную микроскопию. Проще говоря, выявить перекисное окисление липидов. Значение этого диагностического теста не нуждается в объяснении. Ведь в основе значительного количества заболеваний лежит чрезмерная активность перекисного окисления липидов. Выявление этого состояния определяет тактику лечения.
С точки зрения нормальной физиологии перекисное окисление липидов необходимо для образования стероидных гормонов, медиаторов воспаления, цитокинов и тромбоксанов. Но когда количество продуктов обмена данных химических реакций превышает допустимое значение и перекиси повреждают органеллы клетки, нарушают синтез ДНК и белков, в действие вступает антиоксидантная система, снижающая количество свободных радикалов кислорода, ионов металлов с изменчивой валентностью. Кроме этого, она повышает синтез каталазы и пероксидазы с целью утилизации излишков перекисей и продуктов их дальнейшего метаболизма.
Источник
