Одним из первых результатов воспаления является
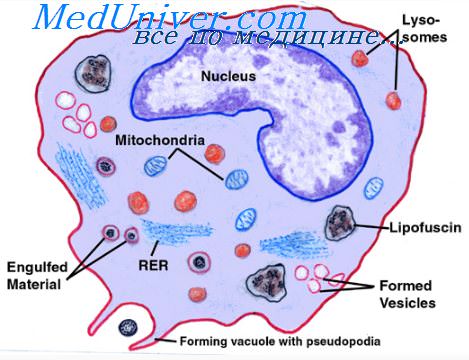
Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
Одним из первых результатов воспаления является «ограждение» области повреждения от остальных тканей. Тканевые пространства и лимфатические сосуды в воспаленной области блокируются сгустками фибрина, поэтому через небольшой промежуток времени жидкость с трудом протекает через интерстиций. Этот процесс отгораживания задерживает распространение бактерий или токсических продуктов.
Интенсивность воспалительного процесса обычно пропорциональна степени повреждения ткани. Например, когда стафилококки проникают в ткани, они выделяют смертельно опасные клеточные токсины. В результате воспаление развивается быстро, гораздо быстрее, чем сами стафилококки могут размножиться и распространиться. Следовательно, для локальной стафилококковой инфекции характерно быстрое отгораживание, предохраняющее от распространения ее по телу.
Стрептококки, напротив, не вызывают такого интенсивного локального разрушения тканей. Следовательно, процесс отгораживания развивается медленно, на протяжении многих часов, в течение которых стрептококки успевают размножиться и мигрировать. В результате стрептококки часто проявляют гораздо более выраженную тенденцию к распространению в организме и развитию смертельных состояний, чем стафилококки, несмотря на то, что стафилококки гораздо более губительны для тканей.

Тканевые макрофаги — первая «линия обороны» против инфекции. В течение нескольких минут после начала воспаления макрофаги, уже присутствующие в тканях, немедленно начинают свое фагоцитарное действие, будь то гистиоциты в подкожных тканях, альвеолярные макрофаги в легких, микроглия в мозге или др. При активации продуктами инфицирования и воспаления первым эффектом является быстрое увеличение каждого из макрофагов.
Затем многие из ранее неподвижных макрофагов отделяются от мест их прикрепления и становятся мобильными, формируя первую «линию обороны» против инфекции в течение примерно первого часа. Количество этих рано мобилизуемых макрофагов часто незначительно, но они спасают жизнь.
Вторжение нейтрофилов в воспаленную область является второй «линией обороны». В течение примерно первого часа после начала воспаления большое число нейтрофилов начинает внедряться в воспаленную область из крови. Этот процесс вызывается продуктами воспаленных тканей, которые инициируют следующие реакции: (1) изменяют внутреннюю поверхность эндотелия капилляров, способствуя прилипанию нейтрофилов к стенкам капилляров в воспаленной области.
Этот эффект, показанный на рисунке, называют маргинацией (или краевым стоянием лейкоцитов), (2) ведут к разрыхлению сцеплений между эндотелиальными клетками капилляров и небольших венул, обеспечивая появление достаточно больших отверстий для прохождения нейтрофилов путем диапедеза непосредственно из крови в тканевые пространства; (3) другие продукты воспаления вызывают хемотаксис нейтрофилов в направлении поврежденных тканей, как объяснялось ранее.
Таким образом, в течение нескольких часов после начала повреждения тканей область обильно заполняется нейтрофилами. Поскольку нейтрофилы крови — уже зрелые клетки, они готовы немедленно начать свои очистительные функции для уничтожения бактерий и удаления инородного материала.
— Также рекомендуем «Нейтрофилия. Защитные механизмы воспаления»
Оглавление темы «Клетки иммунитета. Виды иммунитета»:
1. Ретикулоэндотелиальная система. Макрофаги в лимфатических узлах
2. Альвеолярные макрофаги в легких. Клетки Купфера печени
3. Эффекты воспаления. Макрофаги и нейтрофилы при воспалении
4. Нейтрофилия. Защитные механизмы воспаления
5. Образование гноя. Эозинофилы и базофилы
6. Лейкопения. Лейкемии и его типы
7. Врожденный иммунитет. Приобретенный или адаптивный иммунитет
8. Типы приобретенного иммунитета. Лимфоциты в приобретенном иммунитете
9. Длительность жизни белых клеток крови. Нейтрофилы и макрофаги
10. Роль лимфоцитарных клонов. Происхождение клонов лимфоцитов
Источник
РЕАКЦИЯ ВОСПАЛЕНИЯ — универсальная защитная реакция организма на действие различных патогенных факторов (механических, физических, химических, биологических и др.), благодаря которой происходит обезвреживание и уничтожение вызвавших повреждение факторов. Проникшие патогены индуцируют комплексную реакцию воспаления, которая обеспечивает привлечение лейкоцитов и растворимых компонентов плазмы в очаги инфекции, что приводит к локализации и уничтожению микрорганизмов в области их внедрения.
КЛИНИЧЕСКИЕ ПРИЗНАКИ ВОСПАЛЕНИЯ
· rubor (краснота),
· tumor (опухоль, припухлость),
· calor (жар),
· dolor (боль),
· functio laesa (нарушение функции).
СТАДИИ ВОСПАЛЕНИЯ
В классической патологии было принято выделять три стадии воспаления:
— альтерацию,
— экссудацию,
— пролиферацию.
Такое деление сохраняется и в настоящее время. Однако новые исследования и новые факты показали, что указанные стадии не монолитны, между ними нет четких границ (например, альтерация может быть максимально выражена на стадии гнойной экссудации, а нарушения микроциркуляции могут быть неодинаковыми в одно и то же время в различных участках очага воспаления). Поэтому в зависимости от процесса, преобладающего на определенном этапе воспаления, выделяют следующие стадии (рис.):
Стадия альтерации (повреждения):
· Первичная альтерация
· Вторичная альтерация
Стадия экссудации и эмиграции
Стадия пролиферации и репарации:
· Пролиферация
· Завершение воспаления
Первичная альтерация. Воспаление всегда начинается с повреждения ткани. После воздействия этиологического фактора в клетках происходят структурные, а также метаболические изменения.
Они бывают разными в зависимости от силы повреждения, от вида клеток (степени зрелости) и т.д.
Одни клетки гибнут, другие продолжают жить, третьи даже активируются.
Последние будут играть особую роль в дальнейшем.
Вторичная альтерация. Если первичная альтерация является результатом непосредственного действия воспалительного агента, то вторичная не зависит от него и может продолжаться и тогда, когда этот агент уже не оказывает влияния (например, при лучевом воздействии).
Этиологический фактор явился инициатором, пусковым механизмом процесса, а далее воспаление будет протекать по законам, свойственным ткани, органу, организму в целом.
Действие флогогенного агента проявляется, прежде всего, на клеточных мембранах, в том числе на лизосомах.
Это имеет далеко идущие последствия. Заключенные в лизосомах ферменты реактивны. Но как только лизосомы повреждаются и ферменты выходят наружу, они активируются и усугубляют, то разрушительное действие, которое оказал этиологический фактор. Можно сказать, что первичная альтерация — это повреждение, нанесенное со стороны, а вторичная альтерация — это самоповреждение.
Здесь следует отметить, что вторичная альтерация представляет собой не только повреждение и разрушение.
Некоторые клетки действительно гибнут, другие же не только продолжают жить, но и начинают вырабатывать биологически активные вещества, вовлекая в динамику воспаления иные клетки как в зоне воспаления, так и вне ее.
Клетки воспаления. Макрофаги. Установлено, что активированные макрофаги синтезируют особое вещество, получившее название интерлейкин-1 (ИЛ-1).
Оно выделяется макрофагами в среду и распространяется по всему организму, где оно находит свои мишени, которыми являются миоциты, синовиоциты, гепатоциты, костные клетки, лимфоциты, нейроциты.
По-видимому, на мембранах этих клеток имеются специфические рецепторы, благодаря которым ИЛ-1 действует именно на них, а не на другие клетки. Действие это стимулирующее и более всего изучено применительно к гепатоцитам и лимфоцитам.
Действие ИЛ-1 универсально, т.е. срабатывает при любом инфекционном (воспалительном) заболевании, причем в самом начале, и таким образом дает сигнал указанным органам включиться в воспалительный (инфекционный) процесс.
Есть основание предполагать, что характерные для ранних этапов заболевания симптомы (головная боль, боль в мышцах и суставах, сонливость, лихорадка, лейкоцитоз и увеличение содержания белков, в том числе иммуноглобулинов) объясняется именно действием ИЛ-1 (рис.).
Роль макрофагов не ограничивается секрецией ИЛ-1. В этих клетках синтезируется еще целый ряд биологически активных веществ, каждое из которых делает свой вклад в воспаление. К ним относятся: эстеразы, протеазы и антипротеазы; лизосомальные гидролазы — коллагеназа, аластаза, лизоцим, α-макроглобулин; монокины — ИЛ-1, колониестимулирующий фактор, фактор, стимулирующий рост фибробластов; антиинфекционные агенты — интерферон, трансферрин, транскобаламин; компоненты комплемента: С1, С2, СЗ, С4, С5, С6; дериваты арахидоновой кислоты: простагландин Е2, тромбоксан А2, лейкотриены. Не следует забывать также важнейшую функцию макрофагов — фагоцитоз.
Тучные клетки. Роль этих клеток в воспалении заключается в том, что они при повреждении выбрасывают содержащиеся в их гранулах гистамин и гепарин. А так как эти клетки в большом количестве располагаются по краям сосудов, то и действие указанных веществ проявится, прежде всего, на сосудах (гиперемия).
Макрофаги и лаброциты находятся в тканях постоянно (клетки-резиденты). Другие клетки воспаления проникают в зону воспаления со стороны (клетки-эмигранты). К ним относятся полиморфно-ядерные нейтрофилы, эозинофилы и лимфоциты.
Нейтрофилы. Главная функция этих клеток — фагоцитоз. Они выселяются из костного мозга в кровь, эмигрируют из сосудов и в больших количествах скапливаются в воспаленной ткани.
И активное их размножение, и миграция, и фагоцитоз подвержены регулирующему влиянию биологически активных веществ (тканевых, системных, организменных). Действие их проявляется, однако, только тогда, когда на клетках имеются рецепторы, специфически реагирующие с медиатором воспаления: гистамином, адреналином, глюкокортикоидами, гамма-глобулинами и т.д.
В цитоплазме нейтрофилов имеется два типа гранул: первичные азурофильные (более крупные) — обычные лизосомы, вторичные, или специфические гранулы мельче, а главное, они содержат другой набор ферментных и неферментных веществ. В первичных гранулах содержатся кислые гидролазы, а кроме того, лизоцим, миелопероксидаза и катионные белки. Вторичные гранулы специфические; содержат щелочную фосфатазу, лактоферрин и лизоцим. Все это важно для понимания участия нейтрофилов в воспалении (см. ниже).
Эозинофилы. Роль эозинофилов в воспалении определяется рецепторами, расположенными на поверхности, и ферментами, находящимися внутри. На наружных мембранах имеются рецепторы для комплемента, иммунных комплексов, содержащих IgE, IgG. Из ферментов следует упомянуть гистаминазу и арилсульфатазу В. Важную роль играет большой катионный белок, который способен нейтрализовать гепарин, повреждать личинки ряда паразитов. Миграция и активация эозинофилов происходит под влиянием комплемента (С5а и С5—С7), пептидов тучных клеток, ПГД, веществ, продуцируемых гельминтами.
Тромбоциты. Роль тромбоцитов (кровяных пластинок) в воспалении состоит главным образом в том, что они имеют ближайшее отношение к микроциркуляции. Наверное, это самые постоянные и самые универсальные участники воспаления. В них содержатся вещества, влияющие на проницаемость сосудов, на их сократимость, на рост и размножение клеток, а главное — на свертываемость крови.
Лимфоциты. Эти клетки играют роль при любом воспалении, но особенно при иммунном.
Фибробласты. Действие фибробластов проявляется в последней стадии процесса, когда в очаге воспаления увеличивается число этих клеток, оживляется синтез в них коллагена и гликозамингликанов.
В суммарном виде данные о клетках воспаления представлены в табл. 2.
Медиаторы воспаления. Медиаторами воспаления называются биологически активные вещества, которые синтезируются в клетках или в жидкостях организма и оказывают непосредственное влияние на воспалительный процесс. Клеточные медиаторы были рассмотрены выше (см. табл. 2). Гуморальные медиаторы воспаления синтезируются в плазме и в тканевой жидкости в результате действия соответствующих ферментов. Первоначальной причиной появления (или увеличения количества) этих веществ является альтерация. Именно в результате повреждения клеток освобождаются и активируются лизосомальные ферменты, которые активируют другие ферменты, в том числе содержащиеся в плазме, в результате чего возникает целый ряд биохимических реакций. Поначалу они носят хаотический характер («пожар обмена»), а продукты расщепления не имеют физиологического значения, нередко токсичны. Постепенно, однако, в этом процессе появляется определенный биологический смысл. Протеолитические ферменты расщепляют белки не до конца, а только до определенного этапа (ограниченный протеолиз), в результате чего образуются специфические вещества, действующие целенаправленно и ызывающие специфический патофизиологический эффект. Оказалось, что одни из них действуют преимущественно на сосуды, повышая их проницаемость, другие — на эмиграцию лейкоцитов, третьи — на размножение клеток. Первым обнаружил определенный «порядок» и закономерность в процессе воспаления В. Менкин. В воспалительном экссудате он выявил и индивидуализировал химические вещества и сопоставил с ними определенные слагаемые воспаления: гиперемию, лейкоцитоз, хемотаксис.
Одним из клеточных медиаторов воспаления является гистамин. Он содержится в гранулах тканевых базофилов (тучные клетки или лаброциты) в комплексе с гепарином и химазой в неактивной форме. В. свободном состоянии он оказывает расширяющее действие на мелкие сосуды (капилляры, венулы), увеличивая проницаемость их стенки. В малых дозах гистамин расширяет артериолы, в больших — суживает венулы. Выброс гистамина осуществляется вместе с выбросом в окружающую среду всех или части гранул тканевых базофилов при их дегрануляции. Этому может способствовать воздействие тепла, ионизирующего или ультрафиолетового излучения, растворов солей, кислот, белков, синтетических полимеров и мономеров, поверхностно-активных веществ. Дегрануляция всегда наблюдается при иммунных реакциях, т.е. при взаимодействии антигена с антителом на поверхности тканевых базофилов.
Источник
Введение.
Воспаление является одним из сложных патологических процессов, встречающихся в организме человека и являющихся причиной многих функциональных нарушений в нем. Однако не только сам воспалительный процесс вызывает нарушение функций организма. Эти нарушения могут развиваться в результате последствий воспалительного процесса. Все это заставляет серьезно и вдумчиво отнестись к его изучению.
Проблема воспаления привлекала к себе внимание исследователей с древних времен. Описание внешних признаков воспаления, которые позволили выделить его из числа других патологических процессов, было дано К.Цельсом и Галеном (I-II вв н.э.). «К.Цельс указал на четыре признака воспаления: красноту, припухлость, жар, боль. Позже Гален к этим признакам добавил пятый – нарушение функций».[1] Эти признаки воспаления не утратили своего значения в клинической практике и в настоящее время.
Открытие кровообращения В.Гарвеем явилось основой для объяснения физиологических и патологических процессов в организме. Оно позволило с новых позиций рассмотреть и вопросы воспаления. Теория воспаления, созданная на основе учения В.Гарвея, выдвигала в качестве основного фактора при воспалении нарушение количества содержания крови в сосудах. На основании ряда экспериментов Гунтер пришел к выводу, что при воспалении происходит расширение как венозных, так и артериальных сосудов, объем которых увеличивается.
Первоначально все исследователи, изучавшие процесс воспаления, сводили его исключительно к нарушению кровообращения в тканях и не замечали других явлений при нем. Однако такой односторонний взгляд на процесс воспаления не мог долго держаться в медицине, так как он не отражал действительных изменений в тканях при воспалении и не определял биологической сущности этого процесса.
Вскоре было установлено, что при воспалении наблюдается выход форменных элементов из кровеносных сосудов в очаг воспаления. В самом очаге воспаления было обнаружено наличие нарушений клеточных элементов, которые могли быть активными и пассивными (Р.Вирхов). В понимании Р. Вирхова воспаление представляет собой процесс повреждения клеток с последующим восстановлением их целостности.
«И.И. Мечников существенной стороной процесса воспаления считал фагоцитарную реакцию живого организма на вредные раздражения. Развитие физической и коллоидной химии позволило установить, что в очаге воспаления имеет место ряд физико-химических изменений, которые и определяют развитие основных симптомов воспаления.»[2]
Больные с гнойно-воспалительными заболеваниями составляют треть всех хирургических больных, большинство послеоперационных осложнений связано с гнойной инфекцией.
Современный диапазон хирургических вмешательств (операции на органах брюшной и грудной полости, костях и суставах, сосудах и др.) создаёт опасность нагноений послеоперационных ран, которые нередко приводят к прямой угрозе жизни оперируемых. Более половины всех летальных исходов после операции связано с развитием инфекционных (гнойных) осложнений.
Факторы, определяющие начало развития, особенности течения и исход заболеваний, связанных с воспалением и инфекцией в хирургии:
а) состояние иммунобиологических сил макроорганизма;
б) количество, вирулентность, лекарственная устойчивость и другие биологические свойства микробов, проникших во внутреннюю среду организма человека;
в) анатомо-физиологические особенности очага внедрения микрофлоры;
г) состояние общего и местного кровообращения;
д) степень аллергизации больного.
«За последние годы отмечаются значительные изменения иммунобиологической реактивности населения, вызванные как аллергизирующим влиянием факторов окружающей среды, так и широким применением лечебно-профилактических мероприятий (например, прививки, переливание крови и кровезамещающих жидкостей, лекарственные препараты и т.д.)»[3].
Отмечающееся во всех странах увеличение частоты гнойно-воспалительных заболеваний и послеоперационных осложнений, снижение эффективности их лечения объясняются также быстрым увеличением числа штаммов микроорганизмов, устойчивых к воздействию антибактериальных препаратов.
«Для возникновения гнойного воспаления важно наличие в очаге внедрения микрофлоры мёртвых тканей, т.е. питательной среды для бактерий, и нарушения местного и общего кровообращения (вызванные шоком, острой анемией, сердечной слабостью или другими причинами), затрудняющие доставку в очаг клеточных и химических структур, необходимых для борьбы организма с микробами, создают условия для более тяжёлого течения гнойного процесса»[4].
Выявляется определённая зависимость характера гнойно-воспалительных заболеваний от возраста больных. В молодом возрасте (17- 35 лет) чаще встречаются флегмона, абсцесс, гнойный лимфаденит, мастит, остеомиелит; в возрасте 36-55 лет преобладают заболевания мочевыводящей системы — пиелит, цистит, пиелонефрит, а также парапроктит, перитонит; в возрасте старше 65 лет — карбункул, некротическая флегмона, постинъекционный абсцесс, гангрена и др. У детей гнойная инфекция протекает по типу флегмоны новорождённых, сепсиса, нагноительных заболеваний лёгких и плевры, острого гематогенного остеомиелита, перитонита.
Цель моей курсовой работы – рассмотреть и изучить воспалительные процессы, их классификацию и патогенез; а так же осветить основные принципы местного и общего лечения воспалительных процессов.
Я поставила перед собой задачу: изучить основные методы лечения воспалительных процессов в зависимости от классификации.
Глава 1. Общая патология
Воспаление.
Воспаление — сложный патологический процесс, при котором происходит повреждение тканей с перерождением и отмиранием клеток (альтерация), сосудистые расстройства с выхождением в окружающую ткань жидкой части крови и форменных элементов (экссудация), размножение клеток (пролиферация) в пораженном участке.
В зависимости от свойства и силы воздействующего фактора, величины строения и свойств пораженной ткани и ее реактивности при воспалении могут иметь место самые различные повреждения и изменения в тканях.
«При альтерации может произойти полное омертвение клеток (тканей), нарушение питания тканей или дистрофии различной формы и степени. Одним из первых и основных процессов воспаления является рефлекторное расширение мелких артерий и капилляров, вызванное раздражением нервных окончаний, заложенных в стенках сосудов, или рефлекторно через центральную нервную систему. Вследствие расширения сосудов происходит переполнение их кровью и замедление в них тока крови, что ведет к воспалительной гиперемии. В кровеносных сосудах давление крови повышается, стенки растягиваются и становятся более проходимыми (порозными) для жидкой части крови. Порозность стенок сосудов увеличивается вследствие вызванного воспалительным процессом их изменения.»[5]
Через измененные стенки сосудов в окружающую ткань проникает жидкая часть крови. Этот процесс называется экссудацией, а сама воспалительная жидкость — экссудатом. Чем сильнее повреждена стенка сосуда, тем более крупные белковые частицы она пропускает. Таким образом, от степени повреждения стенки сосудов зависит большее или меньшее содержание белка в экссудате. Известно, что при быстром движении жидкости в трубке взвешенные твердые частицы находятся в середине тока жидкости, а при его замедлении они начинают оседать по стенкам сосуда. То же происходит и с кровью: при нормальном токе крови в сосудах взвешенные форменные элементы крови находятся в середине русла сосуда, а при замедлении тока располагаются ближе к стенкам сосуда. Расположенные у стенки сосуда лейкоциты выпускают, подобно амебам, тончайшие отростки (псевдоподии), проникающие через поры сосудов (мельчайшие щели между клетками эндотелия капилляров).
Через эти отростки все тело лейкоцитов как бы переливается из сосуда в окружающую ткань. Вместе с экссудатом в очаге воспаления скапливается большее или меньшее количество лейкоцитов. Эти лейкоциты, называемые фагоцитами, поглощают отмершие клетки, уничтожают бактерии и продукты их распада; часть лейкоцитов при этом погибает, выделяя при своем распаде особые вещества, которые обезвреживают бактерийные токсины и продукты тканевого распада.
«Значение лейкоцитов в воспалительном процессе и их роль в восстановлении поврежденных тканей открыл известный русский ученый И. И. Мечников. Он говорил, что воспаление нужно рассматривать как фагоцитарную реакцию организма»[6].
В ответ на воспалительный процесс, особенно если последний вызван инфекцией, организм рефлекторно повышает функцию кроветворных органов, которые усиленно вырабатывают лейкоциты, необходимые для осуществления восстановительных процессов.
Кроме лейкоцитов, в воспаленную ткань выходят тромбоциты, а при значительном повреждении сосудистой стенки и эритроциты, которые в момент прохождения через стенку тоже уплощаются и удлиняются. Таким образом, экссудат состоит из белковой жидкости и форменных элементов крови.
Эти примеры еще раз подтверждают основное положение павловского учения о взаимосвязи всех органов между собою в едином целостном организме.
Экссудат отличается от транссудата тем, что возникновение экссудата обусловливается артериальной (а не застойной, венозной) гиперемией и повышенной порозностью кровеносных сосудов, вследствие чего в экссудате обнаруживается большее количество белка (2—4% и больше) и форменных элементов крови.
Формы воспаления и его исходы
В зависимости от характера воспалительного процесса в пораженном органе различают три основные формы воспаления: альтеративное, экссудативное и пролиферативное (или продуктивное).
Альтеративное воспаление характеризуется преимущественно дистрофическими, атрофическими и некротическими процессами. Обычно эта форма встречается в паренхиматозных органах (печени, сердце, почках и др.).
Экссудативная фаза воспаления может иметь следующие виды:
— серозное воспаление (экссудат содержит белок и не содержит форменных элементов крови);
— фибринозное воспаление (экссудат содержит значительное количество фибрина, выпавшего в осадок на ткани);
— гнойное воспаление (в экссудате большое количество лейкоцитов в основном погибших лейкоцитов);
— геморрагическое воспаление (в экссудате много эритроцитов);
— ихорозное воспаление (в экссудате поселяется гнилостная флора).
В процессе развития фазы экссудации в очаге воспаления возникают различные метаболические нарушения. В зоне воспаления:
а)- изменяется газовый обмен, что сопровождается повышением потребления тканями кислорода и уменьшением выделения тканями угольной кислоты, вследствие чего уменьшается дыхательный коэффициент тканей (отношение СО2 к О2). Это свидетельствует о нарушении окислительных процессов в зоне очага воспаления.
б)- нарушается углеводный обмен, что приводит к увеличению в ней содержания глюкозы. Усиление гликолиза способствует накоплению в зоне воспаления молочной кислоты.
в)- повышается содержание свободных жирных кислот, что обусловлено усилением процессов липолиза. Одновременно в тканях накапливаются кетоновые тела.
г)- нарушается белковый обмен, что проявляется накоплением в тканях полипептидов, появлением альбумозы и пептонов.
д)- нарушается минеральный обмен. В экссудате отмечается повышенная концентрация К+, а это способствует еще большему выходу жидкой части крови в ткани и увеличению отека их.
Серозное воспаление сопровождается выделением воспаленной тканью серозного экссудата, состоящего из прозрачной жидкости желтого цвета, иногда с зеленоватым оттенком, содержащей сравнительно небольшое количество лейкоцитов. При воспалении серозных оболочек в плевральной и брюшной полостях может скопляться большое количество жидкости — до нескольких литров.
Гнойный экссудат состоит из богатой белком жидкости, содержащей большое количество лейкоцитов. От примеси лейкоцитов экссудат становится мутным, желтого цвета, а иногда зеленовато- или серовато-желтым. Густой сливкообразный экссудат называется гноем; лейкоциты в гною часто носят название гнойных телец; они являются уже отмершими клетками.
Геморрагический экссудат характеризуется большим содержанием эритроцитов, которых может быть больше, чем лейкоцитов. От примеси красных кровяных телец экссудат бывает розового и даже красного цвета. «Геморрагический экссудат свидетельствует о значительном поражении сосудистой стенки болезнетворным фактором, вследствие чего и происходит выхождение большого количества эритроцитов из кровеносных сосудов»[7].
Гнилостное, или гангренозное, воспаление возникает вследствие проникания в ткань гнилостных бактерий, которые вызывают гнилостный распад тканей с образованием газов зловонного запаха.
Еще один вид воспаления – катаральное; так называют воспаление слизистых оболочек. Катар может быть слизистый, серозный и гнойный. При слизистом катаре воспаленная слизистая оболочка выделяет преимущественно слизь; при серозном катаре на поверхность слизистой оболочки выделяется серозный экссудат, «стекающий» по поверхности слизистой оболочки; при гнойном катаре слизистая оболочка поражается гнойным воспалительным процессом и на ее поверхности выделяется гнойный экссудат.
Фибринозным называется экссудат, богатый белком — фибриногеном, который по выходе из кровеносного сосуда свертывается, образуя фибрин. Часто фибринозный экссудат выделяется на поверхности слизистых и серозных оболочек, образуя фибринозные наложения.
Крупозное и дифтеритическое воспаление является разновидностью фибринозного воспаления, при котором часто наблюдаются довольно значительные повреждения ткани с отложением на их поверхности фибрина в виде отдельных пленок. Экссудативные воспаления встречаются часто не в чистом, а в смешанном виде: серозно-гнойное, серозно-геморрагическое, фибринозно-гнойное, серозно-слизистое и т. д.
В зоне воспаления в результате развивающегося нарушения кровообращения (сдавление тканей в результате отека) и трофических расстройств нервной системы происходит изменение тканевого обмена веществ. Вышедшие из сосудистого русла лейкоциты гибнут, освобождая при этом ферменты, которые начинают переваривать некротизированные ткани. В итоге образуется гнойный экссудат, содержащий большое количество форменных элементов (преимущественно погибших нейтрофильных лейкоцитов) и расплавленные некротизированные ткани. Вследствие развивающего некроза тканей при наличии отграничительного вала вокруг очага воспаления, в центре очага воспаления образуется наполненная гнойным экссудатом полость – абсцесс.
При отсутствии отграничительного вала возникает разлитое нагноение рыхлой клетчатки (флегмона). Гной по межтканевым промежуткам может распространиться в соседние участки, образуя так называемые затеки и натечные абсцессы. При скоплении гноя в естественных полостях организма образуются эмпиемы (эмпиема плевры, желчного пузыря и пр.).
«Для оценки явления, происходящих при воспалении, следует различать те из них, которые носят защитный (приспособительный) характер, и те, которые носят патологический (разрушительный) характер, определяя тем самым вредное действие воспаления»[8].
К защитным реакциям организма на воспаление относятся: 1) артериальная гипертермия; 2) повышение тканевого обмена; 3) эмиграция лейкоцитов; 4) фагоцитоз; 5) общий лейкоцитоз; 6) создание лейкоцитарного и грануляционного вала вокруг очага инфекции; 7) выработка иммунных тел; 8) пролиферация тканей; 9) повышение температуры тканей и пр. Большая часть этих реакций возникает по механизму безусловных рефлексов.
К патологическим реакциям относятся: а) повреждение тканей; б) качественные нарушения тканевого обмена; в) венозная гиперемия и стаз; г) нарушение функции пораженного и отдаленных органов. Эти реакции являются результатом действия патогенного агента и нарушения нервной регуляции тканевого обмена и кровообращения в очаге воспаления.
Благодаря приспособительным реакциям организм в участке воспаления наряду с разрушением клеток и тканей одновременно происходят и восстановительные процессы — восстановление разрушенной ткани за счет размножения новых клеток.
Вследствие указанных процессов («пожирание» фагоцитами отмерших клеток и бактерий, размножение новых клеток) в участке воспаления рефлекторно повышается обмен веществ.
При размножении новых клеток образуется новая соединительная ткань, восполняющая разрушенную ткань; в некоторых случаях такое разрастание бывает чрезмерным. Образование молодой соединительной ткани, так называемой грануляционной, тоже относится к пролиферативным воспалительным процессам.
«Пролиферативная (или продуктивная) форма чаще наблюдается при воспалении межуточной соединительной ткани. Такие воспалительные процессы ведут сначала к увеличению воспаленного органа за счет экссудативных явлений и размножения клеток, а затем вследствие уплотнения и сморщивания соединительной ткани — к его уменьшению»[9]. Это — конечный процесс, уже не воспалительный, а склеротический, или цирротический, которым и завершается воспалительный процесс.
При нахождении в ткани некоторых бактерий (например, туберкулезных палочек), кроме экссудативного, происходит пролиферативное, или продуктивное, воспаление. Грануляционная ткань образуется в виде небольшого узелка, по внешнему виду напоминающего бугорок, или туберкул. Отсюда и произошло название болезни — туберкулез.
Форма воспалительного процесса, свойственная только определенному заболеванию, называется специфическим воспалением.
Так, туберкул — специфический элемент воспаления при туберкулезе, гумма — при сифилисе, специфические узелки и узлы — при проказе.
К смешанным формам воспаления относится и так называемый воспалительный инфильтрат. Он образуется в результате проникания из кровеносных сосудов в пораженный участок преимущественно форменных элементов (лейкоцитов) и в связи с размножением клеток в самой пораженной ткани. Следовательно, при возникновении инфильтрата наблюдаются явления экссудации и пролиферации. Плотная припухлость (иногда ее неправильно называют опухолью) при воспалении является инфильтратом.
«Воспалительные процессы проявляются чрезвычайно разнообразно: в одних случаях преобладают явления альтерации, в других — экссудации, в третьих — пролиферации. Иногда наблюдаются смешанные формы, но во всех воспалительных процессах в большей или меньшей степени встречаются все три элемента воспаления»[10].
Дата добавления: 2016-07-29; просмотров: 1234 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org — Контакты — Последнее добавление
Источник

